BLOQUEANTES NEUROMUSCULARES
Mª
Antuña Braña, Santiago Herrero,
José A Lapuerta. Hospital de Cabueñes. Gijón. Principado de Asturias.
España
INTRODUCCION
Los bloqueantes neuromusculares (BNM) son sustancias
inicialmente naturales, hoy sintéticas, capaces de producir parálisis muscular
actuando en la unión neuromuscular, donde bloquean la transmisión del impulso
nervioso y por tanto la contracción muscular. Estos fármacos son utilizados en
las Unidades de Cuidados Intensivos fundamentalmente para facilitar la
ventilación mecánica en aquellos enfermos críticos, con fallo respiratorio
severo en los que no es suficiente la sedación. Además los nuevos métodos de
soporte respiratorio en el tratamiento del SDRA (PCV, IRV, Hipercapnia
Permisiva, Membrana Extracorporea) han aumentado el uso de estos fármacos ya
que son métodos que exigen una gran
adaptación del enfermo al ventilador lo
cual no siempre se consigue sólo con sedación.
El uso frecuente de los BNM en enfermos
críticos, puso de manifiesto que en este contexto, además de sus efectos
beneficios, también pueden ocasionar
importantes efectos indeseables, entre ellos se debe destacar, por sus
implicaciones posteriores la debilidad muscular prolongada, tema muy
controvertido en la última década. Estos efectos secundarios han condicionado
su uso más restringido. Además es fundamental a la hora de administrar un BNM
en un enfermo crítico, seleccionar aquel fármaco que suponga el máximo beneficio minimizando los riesgos. Debe tenerse
en cuenta que estos fármacos se administran a pacientes que pueden presentar
disfunciones orgánicas y suelen estar recibiendo tratamiento con múltiples
drogas que pueden presentar interacciones con los BNM. El BNM ideal debería ser
de inicio rápido, duración intermedia y predecible para uso en perfusión
continua, no presentar efectos cardiovasculares deletéreos ni en el sistema
nervioso autónomo, no producir liberación de histamina, metabolismo
independiente de función renal o hepática y
tener metabolitos inactivos. En el momento actual todos los nuevos BNM
intentan aproximarse lo más posible al BNM ideal.
CLASIFICACION
Los BNM son clasificados tradicionalmente por
su modo y su duración de acción. Por su modo de acción se distinguen dos tipos:
1. - BNM despolarizantes: Estos mimetizan la acción de la acetilcolina en la unión neuromuscular. Se unen
al receptor de la acetilcolina a nivel postsinaptico lo que da lugar a una apertura inicial de los canales
iónicos (entrada de Na y Ca, salida de K)con despolarización de la placa
motora, produciendo una contracción inicial que se reconoce como
fasciculaciones(cara, manos y pies).Estos fármacos al contrario de la
acetilcolina, que se hidroliza por la acetilcolinesterasa en milisegundos,
terminan su acción cuando difunden fuera de la placa motora, esto causa una
despolarización más prolongada de la placa motora y bloqueo neuromuscular. La
Succinilcolina es el prototipo de estos fármacos.
2. -BNM no
despolarizantes:
Estos compiten con la acetilcolina en los sitios de unión en la placa motora
con lo cual impiden la apertura de los canales iónicos y por tanto la
despolarización y contracción muscular dando lugar a una parálisis flácida. Es
necesario ocupar más del 80% de receptores antes de que la transmisión
neuromuscular se vea afectada (Bloqueo Competitivo)
Los BNM no despolarizantes disponibles en la
clínica se clasifican según su estructura en:
a.- Aminoesteroideos b.-
Benzilisoquinolinas
- Pancuronio -
Tubocurarina (Curare)
- Vecuronio -
Metocurarina
- Pipecuronio -
Mivacurio
- Rocuronio -
Doxacurio
- Atracurio
-
Cisatracurio
Además los BNM pueden clasificarse también
según su duración de acción bloqueante en:
a.- Acción Corta b.-
Acción Intermedia c.-
Acción Larga
- Succinilcolina - Vecuronio - Tubocurarina
- Rocuronio -
Metocurarina
-
Atracurio -
Pancuronio
- Cisatracurio -
Pipecuronio
- Mivacurio -
Doxacurio
INDICACIONES
Las principales indicaciones de los BNM en
las Unidades de Cuidados Intensivos son:
1. - Facilitar la ventilación mecánica,
especialmente en pacientes con SDRA, cuando se emplean técnicas de ventilación
no convencional, que exigen una completa adaptación del enfermo al ventilador y
aún con métodos convencionales siempre que la función respiratoria y
hemodinámica lo demande En esta situación los BNM favorecen el intercambio
gaseoso al anular el trabajo respiratorio, con lo que se mejora la compliance,
además se puede reducir la presión en vías aéreas y la incidencia de
barotrauma.
2. - Disminución del Consumo de Oxigeno en
pacientes con Insuficiencia respiratoria aguda y transporte de oxígeno crítico.
3. - En pacientes con traumatismo
craneoencefálico (TCE), para facilitar el control de la presión intracraneal.
Esta indicación ha estado últimamente cuestionada en relación con la
publicación de algún trabajo en el que se mostraba un aumento significativo de
la morbilidad (estados vegetativos, neumonía, sepsis) en aquellos enfermos con
bloqueo neuromuscular, no obstante alguno de estos trabajos son retrospectivos
y no recogen el modo de administración de los BNM ni la monitorización de los
mismos. Actualmente los BNM no suelen utilizarse de forma sistemática en
paciente con TCE, pero no se cuestiona
su uso en aquellos pacientes ventilados en los que a pesar de dosis adecuadas
de sedación y otras medidas antihipertensión endocraneal permanecen con un
aumento severo de la presión intracraneal, así como en aquellas maniobras que
puedan suponer aumento de la presión intracraneal.
4. - Estado Asmático. El uso de BNM suele ser
él ultimo recurso para intentar controlar la presión en vía aérea,
especialmente elevada en estos pacientes, con el peligro de barotrauma que esto
conlleva. Además el bloqueo neuromuscular es útil para facilitar la
hipoventilación controlada. Deben utilizarse el menor tiempo posible dado el
alto riesgo de complicaciones derivadas del uso conjunto de BNM y corticoides,
piedra angular, estos últimos del tratamiento estado asmático, fundamentalmente
la miopatía esteroidea.
5. – Estado Epiléptico. Los BNM son útiles
para controlar la excesiva actividad muscular existente en estos enfermos.
Pueden utilizarse con la misma finalidad en pacientes con tétanos, hipertermia
maligna o síndrome neuroléptico maligno. Estas indicaciones no presentan
discusión cuando no pueden ser controladas con un tratamiento específico
(anticonvulsivantes, sedantes, magnesio, dantroleno o bromocriptina).
6. -
Facilitar procedimientos
diagnósticos.
7. - Pacientes con gran compromiso del
transporte de oxígeno, para intentar disminuir el consumo de oxigeno
8. - Pacientes seleccionados que deberían permanecer
inmóviles (proteger una intervención quirúrgica o artefacto vascular)
INTERACCIONES
Los BNM son fármacos que se utilizan en pacientes críticos, estos suelen
presentar disfunciones orgánicas así como
alteraciones electrolíticas o del equilibrio ácido-base y habitualmente
reciben tratamiento con múltiples drogas. Todas estas circunstancias pueden
interferir con la farmacocinética y farmacodinámica de los BNM bien potenciando
o antagonizando el efecto de los BNM.
1. - Interacciones
con drogas
a.- Drogas que
potencian la b.-
Drogas antagonistas
acción de los BNM
no despolarizantes
- Anestésicos Halogenados -
Fenitoina
- Anestésicos Locales (Lidocaína) -
Carbamacepina
- Antibióticos -
Teofilina
.Aminoglucósidos (Gentamicina, Tobramicina, Amikacina) - Agentes
Simpaticomiméticos
.Polipeptidos (Polimixina B) -
Corticoesteroides
.Otros antibióticos (Clindamicina, Tetraciclinas)
- Antiarrítmicos
.Procainamida
.Quinidina
.Magnesio
- Antagonistas del Calcio
- Beta-bloqueantes
- Ciclofosfamida
- Dantroleno
- Diuréticos
.Furosemida
.Tiazidas
2.
–Interacciones con condiciones
orgánicas
a.- Condiciones
que potencian b.-
Condiciones que antagonizan
- Alteraciones electrolíticas -
Hipercalcemia
.Hipopotasemia -
Sepsis
.Hipocalcemia -
Politrauma
.Hipermagnesemia -
Quemaduras de alto grado
- Hipotermia -
Fallo hepático con ascitis
- Acidosis Respiratoria -
Hemiplejía
- Miastenia Gravis -
S de denervación
- Síndrome Paraneoplásico -
Neuropatía periférica
.Eaton-Lambert -
Diabetes Mellitus
- Distrofia Muscular
.Enfermedad de Duchenne
- Síndrome Miotónico
.Enfermedad de Steinert
- Esclerosis Múltiple
- Neurofibromatosis
- Porfiria Aguda Intermitente
- ELA
- Poliomielitis
EFECTOS
ADVERSOS DE LOS BNM NO DESPOLARIZANTES
1. - Efectos Cardiovasculares
. Taquicardia e Hipertensión por
bloqueo de R muscarínicos, fundamentalmente con Pancuronio. El Rocuronio puede
tener un mínimo efecto vagolítico
. Hipotensión por vasodilatación
secundaria a la liberación de histamina. Este efecto es más frecuente con los
derivados benzilisoquinolínicos más
viejos como la Tubocurarina, siendo menor con el Mivacurio y el
Atracurio y prácticamente no ocurre con el Cisatracurio y el Doxacurio. La
mayoría de los Aminoesteroideos no liberan histamina.
2. - Debilidad Muscular Prolongada. Se observa en algunos pacientes críticos
después de recibir BNM durante tiempo
prolongado. Es un tema objeto de múltiples publicaciones sobre todo después del
trabajo de Segredo en 1992, en el que aprecia una debilidad muscular prolongada
en pacientes que habían recibido Vecuronio durante tiempo prolongado y además
tenían prácticamente todos ellos insuficiencia renal. Desde entonces numerosos
trabajos han apoyado la relación entre la utilización de BNM no despolarizantes
aminoesteroideos y cuadros de debilidad muscular prolongada, especialmente en
pacientes con insuficiencia renal. Estos cuadros pueden ser potenciados por el
uso conjunto de corticoides. En los últimos años se ha publicado algún caso aislado de debilidad tras la
utilización de Atracurio y algunos autores consideran que este menor número de
casos con el Atracurio puede ser debido en parte a un menor uso del mismo
aunque actualmente se ha generalizado su utilización sobre todo en Europa y los
casos publicados de debilidad muscular prolongada son mínimos.
Otro punto controvertido respecto a la
relación entre debilidad muscular prolongada y uso de BNM es el papel real que
juegan estos en esta debilidad y si se trata tan sólo de un bloqueo
neuromuscular prolongado en pacientes con disfunciones orgánicas que
interfieren la eliminación de los mismos o bien, si ellos por sí mismos tienen
efecto tóxico, potenciando la polineuropatía propia del enfermo crítico o
favoreciendo el desarrollo de miopatía. En relación con la prolongación de
acción de los BNM en pacientes con disfunciones orgánicas, situación frecuente
en enfermos críticos, se esta subrayando en los últimos tiempos la necesidad de
monitorización estrecha de las dosis de BNM para evitar sobredosificaciones,
siendo considerado por la inmensa mayoría de autores, como requisito
indispensable la utilización, en las Unidades de Cuidados Intensivos, de neuroestimuladores periféricos para mantener
un grado de bloqueo óptimo con la mínima dosis necesaria.
Así pues en el paciente crítico la presencia
de debilidad muscular prolongada, aun en presencia de tratamiento con BNM puede
estar en relación con:
1. - Polineuropatía del enfermo crítico
frecuente en pacientes sépticos
2. - Polineuropatía y Utilización de BNM
3. - Miopatía debida a sepsis, BNM y
corticoides, estos presentan clínica y electrofisiológicamente signos de
miopatía primaria con perdida de los filamentos de miosina
La debilidad muscular prolongada es un problema
realmente importante pues supone dependencia de la ventilación mecánica, por
ello es necesario hacer el diagnóstico basándose en la clínica y en los
hallazgos electrofisiologicos. La polineuropatía del enfermo crítico se
manifiesta clínicamente por debilidad de las extremidades y disminución o
abolición de los reflejos tendinosos, con sensibilidad conservada de modo que
él estimulo algésico pude desencadenar gesto facial de dolor, lo cual puede
servir para diferenciar la polineuropatía del bloqueo muscular prolongado, el
cual también afecta a los músculos craneales, no apreciándose entonces gesto de
dolor. No obstante la exploración física con frecuencia es poco fiable, por lo
que deben utilizarse estudios electrofisiologicos. Los hallazgos característicos en la polineuropatía son de forma
precoz (5días) una disminución de la amplitud del potencial de acción,
posteriormente (al cabo de 1-3 semanas) aparecen potenciales de fibrilación y
ondas puntiagudas positivas como signos de denervación. La biopsia muscular
muestra fibras atróficas diseminadas típicas de la denervación aguda o una
atrofia agrupada, característica de la denervación de más larga evolución.
Algunos de estos pacientes presentan una moderada elevación de CPK. Puede haber
necrosis de fibras musculares que sugiere miopatía asociada, secundaria a la
sepsis y al uso de corticoides.
La sepsis puede inducir fundamentalmente una
polineuropatía de la enfermedad crítica que da lugar a una denervación del
músculo y luego en combinación con los corticoides y los BNM a una miopatía. Si
el paciente sobrevive de la sepsis, se produce siempre recuperación del
problema neuromuscular aunque puede requerir varias semanas.
La debilidad muscular prolongada puede
deberse simplemente al defecto de transmisión neuromuscular en especial en
presencia de insuficiencia renal. En pacientes sépticos puede encontrarse
también una miopatía primaria por caquexia o atrofia muscular por desuso y que
también debe tenerse en cuenta a la hora del diagnóstico diferencial de una debilidad
muscular prolongada.
Una complicación rara de la infección es la
necrosis de fibras musculares panfascicular con debilidad generalizada súbita y
aumento de CPK, ocasionalmente mioglobinuria. La recuperación suele ser
bastante rápida y espontánea.
En resumen en el estudio de pacientes críticos con debilidad muscular
que dificulta la desconexión de la ventilación mecánica es importante realizar
una revisión de la historia clínica en relación con sepsis y empleo de fármacos
como los BNM y los corticoides. La
determinación de CPK constituye un
índice aproximado del grado de
destrucción de las fibras musculares, de hecho, algunos autores abogan por la
realización de determinaciones frecuentes de CPK en aquellos enfermos que
reciben tratamiento con bloqueantes neuromusculares. Puede ser necesario además
la realización de una biopsia muscular .Un mismo paciente puede presentar una
combinación de los trastornos antes descritos
MONITORIZACIÓN DE LA FUNCION NEUROMUSCULAR EN UCI
En los pacientes críticos en los que
utilizamos BNM, teniendo en cuenta las importantes complicaciones que pueden
derivar de su utilización, la mayoría de los autores insisten en la necesidad
de monitorizar el grado de bloqueo neuromuscular utilizando neuroestimuladores
periféricos para individualizar las dosis según los requerimientos propios de
cada paciente. La necesidad de esta monitorización ha surgido en los últimos
años en relación con varios estudios americanos de vigilancia del uso de BNM en
enfermos críticos, en los que se observo el desarrollo frecuente de debilidad
muscular y la escasa utilización de neuroestimuladores periféricos en las
Unidades de Cuidados Intensivos.

En teoría cualquier nervio motor periférico
localizado superficialmente puede ser estimulado, sin embargo los diferentes
grupos musculares tienen también diferente sensibilidades a los BNM. Así el
diafragma es el más resistente de todos los músculos, son más sensibles los
otros músculos respiratorios y los músculos de la cara. Los músculos
abdominales y los músculos de las extremidades son los más sensibles. La total
eliminación de la respuesta del nervio facial significa que el diafragma está
paralizado. Dada la accesibilidad de los nervios periféricos se utilizan estos
para la monitorización del bloqueo
neuromuscular y el nervio cubital es el más utilizado.
Los diferentes métodos de neuroestimulación
utilizados incluyen: estimulo simple, estimulo tétanico, estimulación
posttétanica, estimulo en doble salva y el, train-of-four (TOF). El TOF ha
mostrado ser más sensible, especialmente para monitorizar bloqueo neuromuscular
no despolarizante, además es menos doloroso y parece ser el más interesante
para su uso en UCI y el que se utiliza normalmente. Los demás métodos no suelen
utilizarse en UCI y su explicación se sale del objetivo de esta revisión.
Train-of-four(TOF)
Se
utiliza habitualmente el nervio cubital
y se observa la respuesta motora del músculo adductor del pulgar. Aunque la
sensibilidad a los BNM del músculo
adductor del pulgar es mayor que la del diafragma, desde un punto de vista
clínico la presencia de dos respuestas del músculo adductor resultaran en
suficiente parálisis del diafragma para prevenir la tos, hipo y los movimientos
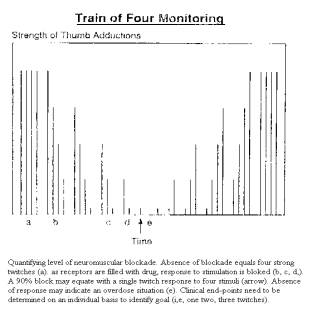
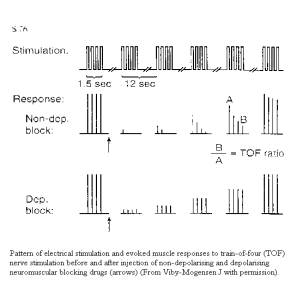
respiratorios durante la ventilación mecánica Durante la realización del TOF se
liberan cuatro estímulos de 2 Hz cada 0,5seg. La respuesta normal son cuatro
contracciones de igual fuerza. Después del bloqueo neuromuscular la fuerza de la contracción muscular disminuye y la
medida de la reducción en la contracción muscular es una expresión del grado de
bloqueo neuromuscular. La respuesta al TOF comienza a disminuir cuando más del
70-75% de los receptores colinérgicos son bloqueados. En presencia de BNM no
despolarizantes, cuyo bloqueo es de tipo competitivo, la fuerza de la
contracción en respuesta a los estímulos decae con cada uno de ellos. Para
medir dicha respuesta muscular a la estimulación se pude recurrir al tacto o
bien se puede objetivar de forma visual mediante la utilización de artefactos
ideados para ello. Una sola respuesta en el TOF implica un 90% de bloqueo
neuromuscular. Se puede medir la ratio entre la respuesta al primer y al cuarto
estimulo. La ratio disminuye en presencia de BNM no despolarizantes. .
La intensidad del estimulo necesaria para
conseguir una respuesta puede variar no siendo nunca menor de 25 mA, pero pude
ser necesario un estimulo más intenso(50-60 mA) en pacientes con aumento de la circunferencia
de la muñeca, por ello se debe realizar una estimulación antes de iniciar el
bloqueo, ya que una inadecuada estimulación con intensidad baja puede conducir
a una sobreestimación del grado de bloqueo y resulta en dosis inapropiadas. Así
pues antes del bloqueo neuromuscular debe ser determinada la estimulación
supramáxima(mA).Esta es definida como el nivel en el cual un aumento adicional
del estimulo no incrementa la respuesta. La estimulación supramáxima suele
estar entre 25-60 mA. Una vez determinada la estimulación supramáxima, esta
será la utilizada en la realización de los siguientes estudios TOF una vez que
se inicia el tratamiento con BNM.
El test TOF debería ser realizado cada hora
hasta que es alcanzada y después cada seis horas. La tasa de infusión se debe
ajustar en función del número de respuestas que se obtienen:
-
Cero respuestas(contracciones): Parar la infusión, restablecerla cuando están
presentes dos respuestas. La tasa de infusión se restaurará en:
.80% si tarda 1 h para recuperar 2 respuestas
.75% si tarda 2 h para recuperar 2 respuestas
.50% si tarda 3 h para recuperar 2 respuestas
.25% si tarda 4 h para recuperar 2 respuestas
-
Una respuesta: Reducir al 80% la dosis presente
-
Dos respuestas: Mantener la misma perfusión
-
Tres respuestas: Mantener la misma perfusión. Aumentar la perfusión un 25% si
el paciente tiene tos, hipo o asincronía con el ventilador
-
Cuatro respuestas: Bolo del 25% de la dosis de carga y aumentar la infusión
25-50%
El TOF pude estar influenciado por la
localización de los electrodos, tipo de electrodos y por la impedancia de los
electrodos y de los tejidos, lo cual ha
de tenerse en cuenta. Debido a este gran número de factores que pueden influir
en los resultados algunos autores han discrepado sobre la utilidad del TOF en
UCI. No obstante la mayoría insisten en la necesidad de monitorizar de la
función neuromuscular mediante los neuroestimuladores y el TOF.
Procedimiento para el TOF
1. - Preparar la piel limpiando con alcohol
2. - Colocar dos electrodos en la superficie
anterior e interna de la muñeca:
a.- Uno se coloca en cara
interna de la muñeca aproximadamente a 1 cm del pliegue de la muñeca
b.- Otro se coloca 2-3 cm
proximal al primero
3. - Colocar el clip del neuroestimulador en
el electrodo
4. - Separar el pulgar del paciente con dos
dedos
5. - Presionar el interruptor del TOF en el
neuroestimulador, comenzar con 25 mA y
sentir el movimiento del pulgar
6. - Si no responde aumentar el miliamperaje para
determinar el estimulo supramáximo y rechequear la respuesta si todavía no hay
respuesta repetir el procedimiento en diferente sitio

PRINCIPALES BLOQUEANTES NEUROMUSCULARES
A.-ACCION CORTA
SUCCINILCOLINA: Bloqueante neuromuscular de
acción ultracorta, es el único BNM despolarizante de uso común en clínica.
Estructuralmente está compuesto por dos moléculas de Acetilcolina (Ach) y
mimetiza la acción de esta en los receptores. El bloqueo neuromuscular despolarizante
se caracteriza por la presencia de fasciculaciones musculares por
despolarización inicial seguido de parálisis flácida por despolarización
mantenida.
La Succinilcolina sufre una rápida metabolización
por la colinesterasa plasmática, por lo que su duración de acción es corta
alrededor de 4-6 min. Aquellas circunstancias que disminuyen la
colinesterasa(enfermedad hepática, mixedema, embarazo, malnutrición, neoplasia)
suponen una prolongación de acción del 50-100%. Un 10% de la droga se elimina
sin cambios por orina. Dosis alta de succinilcolina pueden cambiar el carácter
del bloqueo de despolarizante a no despolarizante.
Este BNM se suele utilizar fundamentalmente
para la intubación urgente, dado su rápido inicio de acción. Con dosis de
intubación 1-1,5 mg/kg se consiguen unas condiciones óptimas para la misma en 20-60 seg.
Su uso más amplio está limitado por sus
efectos adversos:
- Arritmias cardiacas(ritmo de la unión,
parada sinusal, bradicardia o taquicardia)
- Mialgia difusa
- Mioglobinuria (especialmente en niños)
- Hipertermia maligna
- Aumento de presión intraocular,
intragástrica e intracraneal
- Hiperpotasemia. Se puede producir una
hiperpotasemia letal en pacientes con daño neurológico agudo o quemaduras
extensas
Así pues está contraindicada en:
- Quemaduras extensas
- Síndrome de Aplastamiento
- Hipertermia Maligna
- Lesiones de motoneuronas
- Distrofias Musculares
En resumen la Succinilcolina es BNM
despolarizante de ación corta e inicio de acción rápido que se utiliza para la
intubación de urgencia en pacientes que no presentan contraindicaciones.
B.-ACCION LARGA
PANCURONIO: Es el prototipo de BNM no
despolarizante de estructura aminoesteroidea, ha sido uno de los de más amplio
uso en UCI. Es un bloqueante muscular potente, su dosis de intubación es de
aproximadamente 0.06 mg /kg y su inicio de acción comienza a los 2-3 min con
bloqueo máximo a los 4 min, se puede disminuir el tiempo de inicio de acción
aumentando la dosis. Es metabolizado en el hígado en una proporción de un
30-40% dando lugar al 3-OH-pancuronio, metabolito que tiene un 50% de la
actividad bloqueante del pancuronio. Tanto el Pancuronio como su metabolito son
eliminados por orina fundamentalmente y en menor proporción por bilis. Por ello
la duración de acción puede ser prolongada en insuficiencia renal o hepática.
Sus efectos adversos son fundamentalmente
cardiovasculares. Por sus acciones simpaticomimética intrínseca y su efecto
vagolítico pueden producir taquicardia e hipertensión arterial.
Se utiliza en forma de bolos y no suele
utilizarse en perfusión continua debido a su duración de acción que hace
bastante impredecible la duración del efecto bloqueante.
El
pancuronio es un BNM no despolarizante de estructura aminoesteroidea de larga
acción que fue muy utilizado en la UCI en forma de bolos y que actualmente
dados sus efectos cardiovasculares y la disponibilidad de otros más adecuados
está siendo mucho menos utilizado.
PIPECURONIO: Bloqueante neuromuscular no
despolarizante de estructura aminoesteroidea de acción más prolongada que el
pancuronio, pero no esta relacionado con efectos cardiovasculares ni liberación
de histamina. Es ligeramente más potente que el pancuronio con una dosis de
intubación de aproximadamente 0.05 mg/kg. Su inicio de acción es lento
alrededor de 4-5 min. Su duración es de 60-120 min. Un 20% de la droga se metaboliza en el hígado por
desacetilación, el 80% se elimina sin cambios por el riñón al igual que sus
metabolitos, por tanto su duración de acción se prolonga en pacientes con
insuficiencia renal. La experiencia en UCI con el pipecuronio es muy limitada.
El
Pipecuronio es un BNM no despolarizante de acción larga que a pesar de no
presentar efectos cardiovasculares ni liberación de histamina, no suele
utilizarse en UCI, quizá por su acción
demasiado larga.
DOXACURIO: Es un bloqueante neuromuscular
de la familia de las benzilisoquinolinas. Es el BNM no despolarizante más potente,
con una dosis de intubación de 0,03 mg/kg. Es también el de inicio más lento
con un tiempo de inicio de 5-10 min, después de una dosis de intubación. Su
duración de acción es también larga aproximadamente 100-160 min. Su
metabolización hepática es mínima y se elimina en su practica totalidad sin
cambios en orina y bilis. Su efecto es prolongado en pacientes con
insuficiencia renal y menos en pacientes con insuficiencia hepática. El
doxacurio no tiene efectos cardiovasculares y tiene un mínimo efecto en la
liberación de histamina, a pesar de esto su larga acción y poco predecible
duración de acción pueden ser un problema para su uso en UCI. El doxacurio es
un BNM de duración muy larga y de efecto poco predecible lo cual no es muy
adecuado en enfermos críticos, no obstante algunos autores lo recomiendan para
uso en bolo dados sus pocos indeseables en comparación con el pancuronio. En
pacientes con insuficiencia renal se debe disminuir la dosis.
C.-ACCION INTERMEDIA
VECURONIO: Es un BNM no despolarizante de
estructura aminoesteroidea. Su duración de acción es intermedia y puede ser
utilizado en perfusión continua. Su inicio de acción, después de una dosis de
intubación de 0,04 mg/kg, es de aproximadamente 20-40 min. Tiene pocos efectos
colaterales, no altera la función cardiovascular y prácticamente no produce
liberación de histamina. El vecuronio es metabolizado en el hígado por
desacetilación dando lugar a tres metabolitos, 3-OH-vecuronio, 17-OH-vecuronio
y 3,17-OH-vecuronio. El 3-OH-vecuronio tiene una potencia bloqueante de
aproximadamente el 50% del vecuronio, los otros dos metabolitos son inactivos.
Tanto el vecuronio (25%)como sus metabolitos son eliminados por orina. Un 45%
de la droga y un 25% de los metabolitos son eliminados en bilis. En pacientes
con insuficiencia renal el tratamiento con vecuronio durante varias horas o
días puede dar lugar a una parálisis prolongada.
Así pues el vecuronio es un BNM no
despolarizante, aminoesteroideo de amplio uso en UCI por carecer de efectos
cardiovasculares indeseables, además de no producir liberación de histamina. No
obstante presenta el problema de su metabolismo y eliminación órgano
dependiente que ha dado lugar a múltiples casos de debilidad muscular en pacientes con insuficiencia renal, bien
en relación con bloqueo neuromuscular prolongado por lenta eliminación del
fármaco y sus metabolitos o bien por favorecer el desarrollo de polineuropatía
o miopatía dada su estructura esteroidea. Todo ello ha conllevado a que haya
disminuido su utilización.
ATRACURIO: Este es un BNM no
despolarizante con estructura benzilisoquinolinica. Su principal característica
es que tiene un metabolismo órgano independiente, con lo cual no se produzca
acumulación del bloqueante en pacientes con disfunciones orgánicas. Su
metabolización se produce en el plasma por ester hidrólisis y fundamentalmente
por vía Hofmann, esta es una reacción no enzimática que ocurre a temperatura y
pH normal (esta reacción aumenta en pH alcalino). Los metabolitos del atracurio,
laudanosina y acrilatos, no son activos como bloqueantes neuromusculares. La
laudanosina se elimina por vía renal y
puede acumularse en pacientes con fallo renal, esta presenta efectos tóxicos a
nivel del SNC, demostrados en animales en los que produce convulsiones. Es
importante recordar que en humanos no se conocen los rangos tóxicos de
laudanosina, hay alguna evidencia de que el umbral puede ser más alto en
humanos y de hecho son excepcionales las publicaciones de convulsiones con
atracurio. Con respecto a los acrilatos se ha sugerido que pueden producir daño
hepatocelular in vitro, aunque la importancia de esto in vivo permanece sin
aclarar.
El atracurio esta actualmente reconocido como
un buen BNM para uso en UCI. Tiene muy pocos efectos cardiovasculares, excepto
por la liberación de histamina que puede ser considerable sobre todo cuando se
administran dosis altas en bolo rápido, en infusión continua la liberación de
histamina se minimiza. Su inicio de acción tras una dosis de intubación de 0,23
mg/kg es de 3-5 min. Su duración de acción es de unos 20-35 min.
El
atracurio es considerado actualmente como un BNM óptimo para uso en enfermos
críticos ya que está desprovisto de efectos cardiovasculares importantes y la
liberación de histamina es menos importante cuando se utiliza en perfusión
continua, pudiendo limitar, no obstante, su uso en pacientes con broncoespasmo
severo. Además su metabolización órgano
independiente impide su acumulación en pacientes con insuficiencia renal o hepática
evitando problemas de bloqueo prolongado y dado que su estructura no es
aminoesteroidea no conlleva problemas añadidos de miopatía cuando se utiliza
sólo o en combinación con corticoides.
MIVACURIO: Bloqueante neuromuscular no
despolarizante con estructura benzilisoquinolinica. Es el BNM no despolarizante
de acción más corta, alrededor de 15-30 min, no obstante se le suele clasificar
como de acción intermedia. El hecho más interesante respecto al mivacurio es su
metabolización. Es roto en plasma por la colinesterasa plasmática, la tasa de
metabolización depende de la
concentración de mivacurio en
condiciones de cifras normales de colinesterasa. La duración de acción del
mivacurio está prolongada en pacientes con colinesterasa anormal o con colinesterasa
disminuida lo cual puede ocurrir en pacientes con insuficiencia renal.
Con una dosis de intubación de 0,08 mg/kg se
alcanza el máximo efecto a los 3-4 min y su duración de acción es de unos 15
min. Está asociado con liberación de histamina dando lugar a hipotensión y
taquicardia.
Este
BNM no es muy utilizado en el contexto de enfermos críticos por su capacidad
para liberar histamina, no aportando ninguna ventaja importante sobre otros BNM
disponibles en el mercado.
ROCURONIO: Es el BNM no despolarizante de
estructura aminoesteroidea más nuevo. Es un bloqueante poco potente, su dosis
de intubación es de 0,50 mg/kg. Al igual que el vecuronio está casi
completamente desprovisto de efectos colaterales cardiovasculares y no libera
histamina. La principal diferencia con el vecuronio es su inicio de acción
mucho más rápido. Es el BNM no despolarizante de inicio más rápido, tras una
dosis de intubación se consiguen unas condiciones óptimas de intubación a los
60 seg. La eliminación del rocuronio es principalmente a través de la bilis y
algo por vía renal, es muy dependiente de la función hepática para su
eliminación. La duración de acción del rocuronio puede estar prolongada en
pacientes con enfermedad hepática pero podría ser poco afectada en situaciones de
alteración de la función renal.
Actualmente es utilizado fundamentalmente en
anestesia. No existen publicaciones que respalden una cierta experiencia con
este bloqueante en perfusión continua en pacientes críticos. En algún ensayo clínico
aislado se ha apreciado que la perfusión continua con rocuronio puede
proporcionar un buen nivel de bloqueo neuromuscular, pero hay una gran
variabilidad en los requerimientos del bloqueante a lo largo de las horas por
lo que su utilización debería siempre ir acompañado de una monitorización
estrecha de la función neuromuscular con los neuroestimuladores periféricos.
Así pues respecto a este nuevo bloqueante, se
puede concluir que su ventaja de inicio rápido de acción, en el contexto de UCI
pierde importancia y la falta de experiencia con su utilización en perfusión continua, a pesar de su ventaja
teórica en pacientes con insuficiencia renal, no hace aconsejable aún su
utilización de forma habitual.
CISATRACURIO: Es uno de los nuevos bloqueantes
neuromusculares no despolarizantes. Es uno de los 10 esteroisomeros del
atracurio, al igual que este pertenece
a la familia de las benzilisoquinolinas y su metabolización es
principalmente(80%) a través de la vía de Hofmann por lo que no se produce
acumulo en situaciones de disfunción orgánica. Es aproximadamente tres veces
más potente que el Atracurio, por lo que su utilización implica menor
producción de laudanosina y además no produce liberación de histamina.
Existen varios estudios publicados que han
mostrado su utilidad en cuidados intensivos con unos períodos de recuperación
cortos similares a los del atracurio. Su dosis de intubación es de 0,2 mg/kg y
su efecto se produce aproximadamente en 2-3 min. Su duración de acción es de
unos 60 min.
Este nuevo bloqueante neuromuscular parece
reunir todas las características del BNM
óptimo para uso en enfermos críticos, presenta las ventajas del
atracurio de la metabolización y eliminación órgano independiente con lo que no
se produce acumulación en pacientes con disfunción orgánica. Además presenta la
ventaja de no liberar histamina y dado
su potencia los niveles plasmáticos de laudanosina son muy pequeños.
RECOMENDACIONES PARA EL
USO PROLONGADO DE BMN
1. - Usar BNM sólo en pacientes en los que
está estrictamente indicado. El paciente debe estar perfectamente sedado y
analgesiado.
2. - Siempre monitorización del grado
de bloqueo neuromuscular con los neuroestimuladores periféricos y la técnica
del TOF.
3. - Medidas generales: Protección de extremidades, cambios posturales, movilizaciones
pasivas, frecuente lubrificación de los
ojos, profilaxis antitrombotica. Puede ser útil monitorizar CPK.
4. - Evitar el uso conjunto de
corticoides y BNM aminoesteroideos.
5. - Algunos autores recomiendan suspender
diariamente la infusión de BNM, a una
hora determinada, para evaluar la función neuromuscular y la necesidad de
restaurar el tratamiento con BNM. Si esta indicado se inicia nuevamente la
perfusión a la misma dosis, sin precisar bolo. En algunos pacientes esta
practica puede suponer un riego alto de complicaciones.
6. - Seleccionar el agente bloqueante
más adecuado en función de la situación clínica del paciente, buscando siempre
el máximo beneficio con los mínimos riesgos:
a.-
El pancuronio puede ser útil, dado su bajo coste, en pacientes
hemodinámicamente estables y sin
disfunción orgánica, utilizado en forma de bolos. No debe usarse en perfusión
continua.
b.-
El doxacurio, dada su larga duración de acción y al estar desprovisto de
efectos cardiovasculares puede estar indicado en pacientes inestables,
utilizado en forma de bolo.
c.
- En enfermos críticos inestables, sin disfunción renal o hepática, es
preferible el uso de BNM en perfusión
continua pudiendo utilizarse el vecuronio, evitando su utilización combinada
con corticoides.
d.- En pacientes inestables con disfunción
orgánica, deben utilizarse los BNM con eliminación órgano independiente, esto
es el atracurio y el cisatracurio. Este último está especialmente indicado si
la liberación de histamina puede ser un inconveniente.
e.-
En función de los conocimientos y experiencias actuales con BNM, el
cisatracurio puede ser un bloqueante neuromuscular ideal para uso en UCI, ya
que al ser un bloqueante cuya eliminación es órgano independiente no se produce
acumulación en pacientes con disfunción orgánica. Además no libera histamina y
al ser más potente que el atracurio las dosis necesarias son mucho menores y
por tanto los niveles de laudanosina plasmáticos mucho menores.
BIBLIOGRAFIA
-L.
Gramstad, P. Lilleaasen.Neuromuscular blocking effects of atracurium,vecuronium
y pancuronium during bolus and infusion administration.Br J Anaesth
1985;57:1052-1059
-J
Savarese,M. Gargarian,R. Scott et al.Eficacy of atracurium as a cotinius
infusion.Br J Anaesth 1986;58:555
-S.
Williams.Review of atracurium by continous iv infusion.Br J Anaesth
1986;58:551-554
-P.Yate,
P. Flynn, R. Arnold et al. Clinical experience and plasma laudanosine concentrations
during the infusion of atracurium in the intensive therapy unit.Br J Anaesth
1987;59:211-217
-C.
Parker, J. Jones, J. Hunter.Disposition of infusion of atracurium and its
metabolite laudanosine in patients in renal and respiratory faillure in a ITU
.BR j Anaesth 1988;61:531-40
-C.
Parker, J. Hunter.Pharmacokinetics of atracurium and laudanosine in patients
with cirrhosis.Br J Anaesth 1989;62:177-183
-V.
Segredo, M. Matthay, M. Sharma et al.Prolonged neuromuscular blockade after
long-term administration of vecuronium in two critically ill
patients.Anesthesiology 1990; 72: 556-570
-C.
Gwinnutt, J. Eddleston, D. Edwars et al. Concentrations of atracurium and
laudanosine in cerebroespinal fluid and plasma in three intensive care
patients. Br J Anaesth 1990; 65: 829-832
-L.
Brian. Partridge, H. Jerome. Abrams, Carl Bazemore, Roy Rubin. Prolonged
neuromuscular blockade after long-term infusion of vecuronium bromide in the
intensive care unit. Critical Care Medicine 1990; 18: 1177-1179
-J.
Hansen-Flaschen, S. Brazinsky, C. Basile et al. Use of sedating drugs and
neuromuscular blocking agents in patients requering mechanical ventilation for
respiratory failure. Jama 1991; 26: 2870-2875
-S. H.
Subramony, Don E. Carpenter,Seshadri Raju,Marietta Pride. Myopathy and
prolonged neuromuscular blockade after lung trasplant. Critical Care Medicine
1991;19 : 1580-1587
-A.
Rossiter, P. Souney, S. Mc Gowan et al:Pancuronium induced prolonged
neuromuscular blockade. Crit Care Med 1991; 19: 1583-1587
-Beth
A. Vaderheyden,H. Neal Reynolds, Kevin B. Gerold, Tullio Emanuele. Prplonged
paralysis after long-term vecuronium infusion. Critical Care Medicine 1992; 20:
304-307
-M.
Hirano, E. C. Raps, C Minetti, L. Lennihan, N. P. Libbey, E. Bonilla, A. P.
Hays. Acute quadriplegic myopathy: A complication of treatment with steroids,
nondepolarizing blocking agents or both. Neurology 1992; 42: 2087
-V.
Segredo,J. Caldwell, M: A. Matthay et al. Persistent paralysis in critically
ill patients after long-term administration of vecuronium. N Engl J Med 1992;
327:524-528
-D.
Griffin, N. Fairman, D. Coursin et al: Acute myopathy during treatment of
status asthmaticus with corticosteroids and steroidal muscle relaxants. Chest
1992; 102: 510-514
-G.
Benzing, K. Bove. Sedating drugs and neuromuscular blockade during
mechanical ventilation.
Jama1992:
267:1775
-D.
Isenstein, D. Venner, J. Duggan.Neuromuscular blockade in the intensive care
unit. Chest 1992;102:1258-1266
-H.
Klessing, H. Geiger, M. Murray et al.A national survey on the practice patterns
of anesthesiologist intensivists in the use of muscle relaxants. Crit Care Med
1992;20: 1341-1345
-R.
Mirakhur. Newer neuromuscular blocking grugs. An overview of their clinical
pharmacology and therapeutic use. Drugs 1992;44: 182-199
-A. P.
Weeler.Sedation,analgesia, and paralysis in the intensive care unit. Chest
1993;104:566-577
-H.
Rafkin,J. Hoyt.Vecuronium in the intensive care unit: A comparision of
continuos infusion and intermittent boluses. Crit Care Med 1993;21: S 217
-D.
Coursin, M. Murray, Scuder Pet al. An evaluation of doxacurium and pancuronium
in a multicenter, randomized,double-blind study in the criticaly ill.Crit Care
Med 1993;21: S 263
-B. J.
Pollard.Neuromuscular agents in intensive care. Intensive Care Med 1993;19:
S36- S39
-J.
Viby-Mogensen. Monitoring neuromuscular function in the Intensive Care
Unit.Intensive Care Med 1993;19: S74-S79
-C. F.
Bolton. Neuromuscular complications of sepsis.Intensive Care Med 1993; 19:
S58-S63
-Sharon
M. Watling, Joseph F. Dasta. Prolonged paralysis in intensive care unit after
the use of neuromuscular blocking agents: A review of the literature. Critical
Care Medicine 1994;22 : 884-893
-Jeffery
S. Vender. Sedation,analgesia and neuromuscular blockade in critical care:An
overview. New Horizons. 1994; 2: 2-7
-Richard
C. Prielipp, Douglas B. Coursin. Applied pharmacology of common neuromuscular
blocking agents in critical care. New Horizons 1994; 2: 34-37
-John
W. Hoyt. Persistent Paralysis in Critically ill patients after the use of
neuromuscular blocking agents. New Horizons 1993; 2: 48-55
-Judy
E. Davidson. Neuromuscular blockade: Indications, peripheral nerve
stimulation,and other concurrent interventions. New Horizons 1994; 2: 75-84
-John K.
Hsiang,Randall m: Chesnut, Catherine B. Crisp et al. Early routine paralysis
for intrcranial pressure control in severe injury:Is it necessary?. Critical
Care Medicine 1994;22: 1471-1476
-Scott
W Branney, James B. Haenel, Frederick A. Moore et al. Prolonged paralysis with
atracurium infusion: A case report. Crtical Care Medicine 1994; 22: 1699-1701
-Jennifer
M. Hunter. New neuromuscular blocking drugs. The New England Journal of
Medicine 1995; 22: 1691-1699
-Barry
A. Shapiro, Jonathan Warren, Andrew B. Egol et al.Practice parameters for
sustained neuromuscular blockade in the adult critically ill patient: An
executive summary. Cirtical Care Medicine 1995;23: 1601-1605
-Michael
J. Murray, Douglas B. Coursin, Phillip E. Scuderi et al. Double -blind,randomized,multicenter
study of doxacuium vs pancuronium in intensive care unit patients who require
neuromuscular blocking agents. Critical Care Medicine 1995; 23: 450-458
-M. A.
Estecha Foncea, C. A. De la Cruz Perez, C. Chamorro Jambrina, M. A. Romera
Ortega. Uso racional de los bloqueantes neuromusculares en la Unidad de
Cuidados Intensivos. Medicina Intensiva 1995; 19: 371-378
-Robert
N. Sladen. Neuromuscular blocking agents in the Intensive Care Unit: a
Two-edged sword (editrials).Critical Care Medicine 1995; 23: 423-427
-Rodger
E. Barnette, David J. Fish. Monitoring neuromuscular blockade in the critically
ill(Letters to the Editor). Critical Care Medicine 1995; 23: 1790-1791
-Richard
C. Prielipp, Douglas B. Coursin, Phillip E. Scuderit et al. Comparision of the
infusion requirements and recovery profiles of vecuronium and cisatracurium in
Intensive Care Unit patients. Anesth Analg 1995; 81:3-12
-A. J.
Pearson, N. J. N. Harper, B. J. Pollard. The infusion requirements and recovery
chacacteristics of cisatracurium or atracurium in intensive care patienets.
Intensive Care Medicine. 1996; 22: 694-698
-A. M.
De Wolf, J. A. Freeman, V. L. Scott et al. Pharmacokinetics and
pharmacodynamics of cisatracurium in patients with end-stage liver diseasa
undergoing liver transplantation. British Journal of Anaesthesia 1996; 76:
624-628
-Marcie
A. Rubin, Nichocolas Sadovnikoff. Neuromuscular blocking agents in the
Emergency Medicine 1996; 4: 193-199
-Julian
Bion, Richard C. Prielipp, David Bihari et al. Cisatracurium in intensive care.
Current Opinion in Anaesthesiology 1996;9(suppl1): S47-S51
-Karin
S. Khuenl-Brady, Harald J. Sparr, Ursula Waibel. Neuromuscular blocking agents
in the Intensive Care Unit:A Two-Edwed Sword.(Letters to the Editor). Critical
Care Medicine 1996; 24: 717
-J. J.
Savarese, H. Deriaz, H. Mellinghoff, E. G. Pavlin, M. D. Sokoll. The
pharmacodinamics of cisatracurium in healthy adults. Current Opinion
Anaesthesiology 1996; 9 (Suppl1): S16-S22
-J. J.
Savarese, J. Viby-Mogensen, D. Reich, H. Van Aken. The haemodynamic profile of
cisatracurium. Current Opinion Anaesthesilogy 1996; 9(Supply1):S36-S41
-D. F.
Kisor, V. D.Schmidt, W. A. Wargin, et al. Importance of the organ-independent
elimination of cisatracurium.Anesthesia Analg 1996; 83: 1065-1071
-A. H.
Boyd, N. B. Eastwood, C. J. R. Parker, J. M. Hunter. A comparision of the
pharmacodynamics and pharmacokinetics of an infusion of cisatracurium or
atracurium in critically ill patients undergoing mchanical ventilation in the
intensive therapy unit. Br J Anaesth 1996; 76: 382-388
-Robert
J. Colosimo, John V. Levon. Cisatracurium.The newest nondepolarizing
neuromuscular blocking. P&T 1997: 23-29
-J. C.
Lopez Rivas, M. Garcia Viada, J. Serrano Molina. Bloqueantes neuromusculares.
Recomendaciones para su uso en Unidades de Transporte Asistido. Emergencias
1997; 9: 103- 107