- Se conoce que el citrato es un potente inhibidor de la formación de cálculos renales9. En la orina hay varias sustancias que facilitan la formación de complejos solubles con los cationes y que se conocen genéricamente como inhibidores de la cristalización. La disminución o ausencia de estos inhibidores facilita la formación de cálculos. El citrato retarda la cristalización de las sales de calcio a través de dos mecanismos: a) forma complejos con el calcio y reduce la concentración de calcio iónico en la orina; b) el citrato inhibe directamente la cristalización del oxalato cálcico y el fosfato cálcico1,2,10,11
- La dosificación del citrato urinario es actualmente un método fácil y que puede aplicarse en la mayoría de laboratorios. El citrato urinario se mide por medio de un kit (Boehringer Manheim) con un método enzimático.
- La hipocitraturia es un hallazgo frecuente en pacientes con litiasis renal oxalato-cálcica12. Existen numerosos artículos que muestran que el descenso del citrato urinario en pacientes con litiasis renal varía entre un 19% y un 63%2,6. En el estudio de Dallas la hipocitraturia aislada se halló en el 5% de los pacientes, y asociada a otras anomalías en un 50% de los pacientes con litiasis.
- Existe un amplio conocimiento acerca del metabolismo del citrato y de sus mecanismos de acción.
- Diversos tests permiten valorar el riesgo litógeno de los pacientes y su corrección con medidas terapéuticas 15
- PAK CYC. Citrate and renal calculi. New insighits and future directions. Amer J Kidney Dis 1991; 17: 420
- PAK CYC, ADAMS BV. Potassium citrate therapy of nephrolithiasis. En: Renal stone disease. Martinus Nijhotf Publishing, Boston 1987; 201-224
- NICAR, MJ, HSU, MC; FETNER, C. Urinary response to oral potassium citrate therapy for urolithiasis in a private practice setting. Clin Ther 1986; 8: 219
- PREMINGER GM, SAKHAEE K, SKURLA C, PAK CYC. Prevention of recurent calcium stone formation with potassium citrate therapy in patients with distal renal tubular acidosis. J Urol 1985; 134: 20
- GREGORY JG, PARK KY, WILT R, FEIGEL A. Therapy for enteric hyperoxaluria: A comparison of calcium supplementation and urinary alkalinization. En: Urolithiasis. Clinical and Basic Research. LH Smith, WG Robertson, B Finlayson (Eds). Plenum Press, New York 1981; 179-190
- PAK CYC, FULLER C, SAKHAEE K, PREMINGER GM, BRITTON F. Long-term treatment of calcium nephrolithiasis with potassium citrate. J Urol 1985; 134: 11
- BARCELÓ P, WUHL 0, SERVITGE E, ROUSAUD A. Litiasis oxalato cálcica hipocitraturia. Tratamiento con citrato potásico. En: Urolitiasis, metodologfa diagnóstica y terapéutica. A. Rousaud y P. Barceló (Eds). Pulso Ediciones, Barcelona 1992; 67-75
- BARCELÓ P, WUHL O, ROUSAUD A. Hipocitraturia y litiasis renal. Actas Fundació Puigvert 1990; 2: 75
- AZOURY R. GARSIDE J, ROBERTSON WG. Calcium oxalate precipitation in a flow system. J Urol 1981; 136: 150
- MEYER JL, SMITH LH. Growth of calcium oxalate crystals. II. Inhibition by natural urinary crystal growth inhibithors. Invest Urol 1975; 13: 36
- KOK DJ, PAPADOULUS SE, BIJVOLT OL. Excessive crystal agglomeration with low citrate excretion in recurrent stone-former. Lancet 1986; 1: 1056
- CONTE A, GIANOTTI M, GRASES F. On the relation between citrate and calcium in normal and stone-former subjects. Int Urol Nephrol 1989; 21: 369
- HAMM LL. Renal handling of citrate. Kidney Int 1990; 38: 728
- TORRES A, SURIA S. Avances en la patogénesis de la nefrolitiasis cálcica. Nefrología 1990; 2: 119
- CONTE A, PIZA A, GARCÍA-RAJA A, GRASES F, COSTA-BAUZA A, PRIETO MR. Urinary lithogen risk test: usefulness in the evaluation of renal lithiasis treatment using crystallization inhibitors (citrate and phytate). Arch Esp Urol, 1999 52: 305-310
- PAK CYC. Hypocitraturic calcium nephrolithiasis. En: Urolithiasis. A medical and surgical reference. WB Saunders Company, Philadelphia 1990; 89-103
- ALBRIGHT F, CONSOLAZIO WV, COOMBS FS. Metabolic studies and therapy in a case of nephrocalcinosis with rickets and awarfism. Bull Johns Hopkins Hosp 1940; 66: 7
- KISSIN B, LOKS MD. Urinary citrates in calcium urolithiasis. Proc Soc Exp Biol Med 1941; 46: 216
- HOWARD JE. Clinical and laboratory research concerning mechanisms of formation and control of calculous disease of the kidney. J Urol 1954; 72: 999
- BUTZ M, DULCE HJ, Enhancement of urinary citrate in oxalate stone formers by the intake of alkaline salts. En: Urolithiasis. Clinical and Basic research. Smith L, Robertson WG, Finlayson B. Plenum Press, New York 1981; 881-884
- SAKHAEE K, NICAR M, HILL K, PAK CYC. Contrasting effects of potassium citrate and sodium citrate therapies on urinary chemistries and crystallization of stone-forming salts, Kidney Int 1983; 24: 348
- PAK CYC, SAKHAEE E, FULLER CJ. Physiological and physicochemical prevention of calcium-stone formation by potassium citrate therapy. Trans Assoc Am Physicians 1983; 96: 294
- CICERELLO E, MERLO F, GAMBARO G, MACCATROZZO L, FANDELA A, BAGGIO B, ANSELMO G. Effect of alkaline citrate therapy on clearance of residual stone fragments after extracorporeal shock wave litotripsy in sterile calcium and infection nephrolithiasis patients. J Urol 1994; 151: 5
- GELONCH G, FERNÁNDEZ L. Análisis coste-efectividad del tratamiento preventivo de recidivas de litiasis urinaria con citrato potásico. Arch Esp Urol, 1997 50: 373-380
- ÁLVAREZ MV, TRABA ML, RAPADO A.: Metabolismo del ácido cítrico. Su interés en la clínica. Rev Clin Esp 1992; 191: 343
- BARUCH SB, BURICH RL, EUN CK, KING VF. Renal metabolism of citrate. Med Clin N Am 1975; 59: 569
- NIETH H, SCHOLLMEYER, P. Substrate-utilization of the human kidney. Nature 1966;209:1244
- VAES GM, NICHOLS G. Metabolic studies of bone in vitro. III. Citric acid metabolism and bone mineral solubility. Effects of parathormone and stradiol. J Biol Chem 1961; 236: 3323
- COWLEY DM, MC WHINNEY BC, BROWN JM, CHALAMERA AH. Chemical factors important to calcium nephrolithiasis: evidence for impaired hydrocarboxylic absorption causing hyperoxaluria. Clin Chem 1987; 33: 243
- RUDMAN,D, DEDONIS JL, FOUNTAIN ML, CHANDLER JB, GERRON GG, FLEMING GA, KUTNER MH. Hypocitraturia in patients with gastrointestinal malabsorption. N Engl J Med 1980; 303: 657
- OH MS. A new method for stimating G-I absorption of alkali. Kidney Int 1989; 36: 915
- PAK CYC. Hipocitraturia y litiasis renal. En: Urolitiasis, metodología diagnóstica y terapéutica. A Rousaud y P Barceló (Eds) Pulso Ediciones, Barcelona 1992; 57-65
- BRESLAU NA, BRINKLEY L, HILL KD, PAK CYC. Relationship of animal protein-rich diet to kidney stone formation and calcium metabolism. J Clin Endocrinol Metab 1988; 66: 140
- GRASES F, PRIETO R, TUR JA. Dietary effects upon calcium oxalate urolithiasis risk. Int Urol Nephrol 1992; 24: 495
- SIMPSON DP. Citrate excretion a window on renal metabolism. Am J Physiol 1983; 244: F223
- BRENNAN TS, KLAHR SW, HAMM LL. Citrate transport in rabbit nephron. Am J Physiol 1986; 251: F683
- GROLLMAN AP, WALKER WG, HARRISON HC, HARRISON HE. Site of reabsorption of citrate and calcium in the renal tubule of the dog. Am J Physol 1963; 206: F697
- WRIGHT SH, KIPPEN L, KLINENBERG JR, WRIGHT EM. Specifity of the transport system for tricarboxylic acid cycle intermediates in renal brush border. J Membr Biol 1980; 57: 73
- SHERIDAN E, RUMRICH G, ULLRICH KJ. Reabsorption of dicarboxylic acids from the proximal convolution of the rat kidney. Pflugers Arch 1983; 399: 18
- ULLRICH KJ, FASOLD H, RUMRICH G, KLOSS S. Secretion and contraluminal uptake of dicarboxylic acids in the proximal convolution of rat kidneys. Pflugers Arch 1984; 400: 241
- CRAWFORD MA, MILNE MC, SCRIBNER BH. The effects of changes in acid base balance on urinary citrate in the rat. J Physiol 1959; 149: F413
- ADLER S, ANDERSON B, ZEMOTEL L. Metabolic acid-base effects on tissue content and metabolism in the rat. Am J Physiol 1971; 220: F986
- BARAC-NIETO M. Effect of PH, calcium, and succinate on sodium citrate contransport in renal microvilli. Am J Physiol 1984; 247: F282
- FOURMAN P, ROBINSON JR. Disminished urinary excretion of citrate during deficiencies of potassium in man. Lancet 1953; 11: 656
- HARVEY JA, ZOVITZ MM, PAK CYC. The relationship of strogen and progesterone to urinary citrate excretion. J Lithotr Stone Dis 1989; 1: 204.
- REICHEL H, KOEFFLER PH, NORMAN AW. The role of the vitamin D endocrine system in health and disease. N Engl J Med 1989; 320: 990
- FOURMAN P, McCONCEY B, SMITH JWG. Deftects of water reabsorption and of hydrogen-ion excretion by the renal tubules in hyperparathyroidism. Lancet 1960; ii: 619
- HODGKINSON A. The relation between citric acid and calcium metabolism with particular reference to primary hyperparathyroidism and idiopathic hypercalciuria. Clin Sci 1963; 24: 167
- ALVAREZ-ARROYO MV, TRABA ML, RAPADO A, DE LA PIEDRA C. Role of citric acid in primary hyperparathyroidism with renal lithiasis. Urol Rev 1992; 20: 88
- BARCELÓ P, LOPEZ-LILLO J, FERRÉ J, SANTAULARIA JM, DEL RIO G. Hiperparatiroidismo primario. Balance Ca-P postparatiroidectomia. Rec Clin Esp 1985; 176: 9
- GORDON EE, SHEPA SG. Effect of acetazolamide on citrate excretion and formation of renal calculi. Report of a case and study of five normal subjects. N Engl J Med 1957; i: 1215
- SIMPSON DP. Effect of acetazolamide on citrate excretion in the dog. Am J Physiol 1964; 206: 883
- BRECEVIC, L, FUREDI-MILHOFER H. Precipitation of calcium phosphates from electrolyte solutions. V. The influence of citrate ions. Calcif Tissue Int 1979; 28: 131
- GATT S, BARENHOLTZ Y. Enzymes of complex lipid metabolism. Ann Rev Biochem 1973; 42: 61
- KHANNIAZI UK, KHANAM A, NAQUI SA, SHEIKH MA. Study of potassium citrate treatment of crystalluric nephrolithiasis. Biomed Pharmacother 1993; 47: 25
- 0STHER PJ, BOLLERSLEV J, HANSEN AB, ENGEL K, KILDEBERG P. Pathophysiology of incomplete renal tubular acidosis in recurrent renal stone formers evidence of disturbed calcium, bone and citrate metabolism. Urol Res 1993; 21: 169
- RESTAINO I, KAPLANB S, STANLEY C, BAKER L. Nephrolithiasis, hypocitraturia and a distal renal tubular acidificacion defect in type I glycogen storage disease. J Pediatr 1993; 122: 392
- YAMAGUCHI S, KOIDE T, UTSUNOMIYA M, YOSHIOKA T, OKUYAMA A. The effects of long-term alkali therapy for recurrent stone patients with distal renal tubular acidosis. Nippon Hinyokika Gakkai Zasshi 1993; 84: 674
- TUNSSANGA K, SRIBOONLUE P, BORWORNPADUNGKITTI S, TOSUK HOWONG P, SITPRIJA V. Urinary acidification in renal stone patients from northeastern. Thailand J Urol 1992; 147: 328
- PAK CYC. Citrate and renal calculi. Miner Electrolyte Metab 1987; 13: 257
- NICAR MJ, PETERSON R, PAK CYC, Use of potassium citrate as potassium supplement during thiazide therapy of calcium nephrolithiasis. J Urol 1984; 131: 430
- PREMINGER GM. Renal calculi: Pathogenesis, diagnosis and medical therapy. Semin Nephrol 1992; 12: 200
- MARTINI LA, CUPPARI L, CUNHA MA, SCHOR N, HEILDELBERG IP. Potasium and sodium intake and excretion in calcium stone forming patients. J Ren Nutr 1998; 127-31
- PAK CYC, PETERSON R. Succesful treatment of hyperuricosuric calcium oxalate nephrolithiasis with potassium citrate. Arch Intern Med 1986; 146
- HOSKING DH, ERICKSON SB, VAN DEN BERG CJ, WILSXON DM, SMITH LH. The stone clinic effect in patients with idiopathic calcium urolithiasis. J Urol 1983; 130: 1115
- ABDULHADI MH, HALL PB, STREEM SB. Can citrate therapy prevent nephrolithiasis? Urology 1993; 41: 221
- BARCELO P, WUHL 0, SERVITGE E, PAK CYC. Randomized double-blind study of potassium citrate in idiopathic hypocitraturic calcium nephrolithiasis. J Urol 1993; 150: 1761
- PINTO B, CRESPI G, SOLE-BALCELLS F, BARCELÓ P. Patterns of oxalate metabolism in recurrent oxalate stone formers. Kidney Int 1974; 5: 285
- BARCELÓ P, PINTO B. Mineral metabolic studies in renal lithiasis. En: Urinary Calculi. Recent Advances in Aetiology; stone structure and Treatment. L. Cifuentes, A. Rapado, A. Hodgkinson (Eds) S Karger, New York 1973; 149-151
- BARCELO P. Metodologia diagnóstica en la nefrolitiasis metabólica. Laboratorio 1990; 58: 33
- SUZUKI K, TSUGAWA R, RYALL RL. Inhibition by sodium-potassium citrate (CG-120) of calcium oxalate crystal growth on to Kidney stone fragments obtained from extracorporeal shock wave lithotripsy. Br J Urol 1991; 68: 132
- PAK CYC. Hypocitraturic calcium nephrolithiasis. En: Urolithiasis, a Medical and Surgical Reference. MI Resnick CYC Pak (Eds) WB Saunders, Philadelphia 1990; 89-103
- PREMINGER GM, SAKHAEE K, PAK CYC. Alkali action on the urinary crystallization of calcium salts. Contrasting responses to sodium citrate and potassium citrate. J Urol 1988; 139: 240
- SAKHAEE K, ALPERN R, JACOBSON MR, PAK CYC. Contrasting effects of various potassium salts on renal citrate excretion. J Clin Endocrinol Metab 1991; 72: 396
- WABNER CL, PAK CYC. Effect of orange juice consumption on urinary stone risk factors. J Urol 1993; 149: 1405
- COE FL, PARKS JH, WEBB DR. Stone-forming potencial of milk or calcium fortified orange juice in idiopathic hypercalciuric adults. Kidney Int 1992; 41: 139
- PREMINGER GM, SAKHAEE K, PAK CYC. Hypercalciuria and altered intestinal calcium absorption ocurring independently of vitamin D in distal renal tubular acidosis. Metabolism 1987; 36: 176
- SLANINA P, FRECH W, BKOSTROM L.. Dietary citric and enhances absortion of aluminium in antiacids. Clin Chem 1986; 32: 539
- MOLITORIS AB, FROMENT DH, MACKENZIE TA, HUFFER WH, ALFREY,AC. Citrate: A major factor in the toxicity of orally administered aluminium compounds. Kidney Int 1989; 36: 949
PANEL DE DISCUSION |
Litiasis renal
Metabolismo de los citratos y su empleo terapéutico
P. Barceló
Servicio de Nefrología. Fundació Puigvert. Barcelona
El empleo del citrato potásico en la profilaxis de la litiasis renal no se inicia de forma reglada, hasta 1985. En este año la Food and Drug Administration aprueba el tratamiento con citrato potásico en pacientes con nefrolitiasis recidivante1. Antes, los pacientes con litiasis eran tratados con jarabe de citrato potásico2, lo que ocasionaba intolerancias digestivas y su aplicación se reducía a un número escaso de pacientes. La introducción de la Wax-matrix de citrato potásico (WMCP) evitó su intolerancia digestiva y propició su empleo clínico. Esta forma galénica, estudiada en Tejas, consiste en una matriz de cera carnauba, semejante a un panal de abeja, en la que se introduce el citrato que se libera lentamente y no irrita el tracto digestivo. La eficacia de esta droga en la litiasis renal viene avalada por diversos estudios que muestran una reducción de la actividad de la litiasis con el nuevo tratamiento3-5
La acidosis tubular renal, el síndrome diarreico crónico, la litiasis cálcica hiperuricosúrica, la hipocitraturia esencial o secundaria a tiazidas y la hipocitraturia-hipercalciuria son entidades que han sido tratadas con citrato potásico con resultados satisfactorios. Las dosis terapéuticas varían entre 20 y 100 mEq/día y con ellas se pretende aumentar la concentración de los citratos y mejorar la solubilidad urinaria. La dosis empleada depende del grado de hipocitraturia. En pacientes con niveles urinarios inferiores a 100 mg/día suele iniciarse la terapéutica con una dosis repartida de 60 mEq/día y a los 3-4 meses se efectua un reajuste de la dosis según el efecto obtenido6-8.
El interés que ha despertado esta terapéutica se debe a una serie de razones:
Durante la última década numerosos artículos sobre este tema ponen de manifiesto el interés por el citrato, su mecanismo de acción, metabolismo y terapéutica2,6,13,14. No obstante, el potencial terapéutico de este álcali fue apreciado bastantes años antes. Para una adecuada perspectiva del citrato y su relación con la litiasis renal, una breve reseña histórica de esta "nueva droga" nos ayudará a comprender el olvido del citrato potásico en la terapéutica de la litiasis renal cálcica.
REVISIÓN HISTÓRICA
Aunque el desarrollo de la terapéutica con citrato potásico en la nefrolitiasis se atribuye al estudio de Dallas, en realidad sus orígenes se remontan al siglo pasado: Sir Astley Cooper, médico de la reina de Inglaterra, en 1826 prescribía licor de potasio para los cálculos renales cuya composición era presumiblemente de ácido úrico16. En 1940 Albright trata con una mezcla de citrato sódico y ácido cítrico una paciente con osteomalacia y acidosis tubular renal17. Kissin y Locks describen en 1941 una disminución en la excreción de citratos urinarios en pacientes con litiasis cálcica y sugieren que la hipocitraturia urinaria interviene en la formación de cálculos18. El tratamiento con citratos, por tanto, podría prevenir la recidiva calculosa. Años más tarde (1954) J.E. Howard emplea una mezcla de citrato sódico y citrato potásico en el tratamiento alcalinizante de pacientes con litiasis úrica y cistínica19. En 1981 G. Gregory alcaliniza la orina de litiásicos con hiperoxaluria secundaria a una hiperabsorción intestinal del oxálico y observa la reducción del calcio urinario y la disminución de la insolubilidad urinaria del oxalato cálcico5. Este efecto se atribuye a un aumento del citrato urinario que evita la cristalización del oxalato cálcico. M. Butz y J. Dulce demuestran que la alcalinización urinaria con una mezcla de citrato sódico y citrato potásico provoca una caída del calcio urinario y un ascenso de los citratos en litiásicos recidivantes con eliminación de cálculos de oxalato-cálcico20. En 1983, K. Sakhaee y colaboradores, describen los mecanismos de acción del citrato potásico y el citrato sódico21. El citrato potásico provoca una disminución del calcio urinario y del producto de saturación del oxalato cálcico; además aumenta la actividad inhibitoria contra la cristalización del oxalato cálcico, mientras que el citrato sódico no altera el calcio urinario ni tiene ningún efecto inhibitorio sobre la cristalización del oxalato cálcico o el fosfato cálcico. Estos datos explican que al tratar la litiasis úrica con citrato sódico pueda provocarse, en algunos enfermos, la formación de cálculos cálcicos.
En 1983 Pak emplea la terapéutica con citrato potásico en la prevención de la litiasis oxalato-cálcica y sugiere que esta terapéutica podría causar la disolución de los cálculos cálcicos en litiásicos22. Recientemente se ha publicado un artículo que muestra los efectos beneficiosos del citrato potásico en la expulsión de fragmentos de cálculos después de una sesión de litotricia23.
A partir de 1990 el citrato potásico es empleado en numerosos pacientes con litiasis renal con buenos resultados y también para la eliminación de restos calculosos post-litotricia.
METABOLISMO DE LOS CITRATOS
El citrato es un ácido tricarboxílico con un pKa de 2,9, 4,3 y 5,6 y es el componente esencial del ciclo del ácido tricarboxílico a nivel intracelular. Constituye una importante fuente de energía. Estudios en humanos revelan que el citrato proporciona alrededor del 10% de la energía que se consume en el proceso oxidativo renal. La investigación animal muestra unos resultados semejantes13,23. Baruch midió la producción de C02 en el riñón de perro después de infundir citrato marcado (C14 citrato) y comprobó que la energía proporcionada por la vía del ácido cítrico era del 15%26. Nieth y Shollmeyer describieron que el citrato produce el 10% de la energía que precisa el riñón humano. La mayoría del citrato es metabolizado celularmente, es depositado en el hueso y éste constituye su principal reservorio25,28. Se utiliza preferentemente en dos órganos, hígado y riñón, que elimina sólo el 0,7% del citrato total. En el plasma los niveles de citrato son bajos, con unas concentraciones de unos 0,44 mM. La mayoría del citrato plasmático está en forma de anión trivalente (citrato-3) dado que su pKa de 5,6 es bastante inferior al pH fisiológico. La concentración de citrato plasmático como anión trivalente (citrato-3) prácticamente no varía con los cambios del pH plasmático; sin embargo, el citrato en forma de anión divalente (citrato-2) sufre cambios importantes con la variación del pH. Ambas formas (citrato-2 y citrato-3) mantienen unos niveles plasmáticos que no se modifican con la ingestión de este ácido tricarboxílico y sólo se producen aumentos transitorios después de una sobrecarga oral de citrato29. El citrato plasmático se halla en dos formas: una libre y otra unida al calcio, magnesio y sodio. La forma libre es filtrada por el glomérulo y aparece en la orina en cantidades poco variables.
Absorción intestinal del citrato. Factores reguladores
La relativa independencia de los niveles plasmáticos de citrato con los aportes alimentarios parece debida a que el citrato absorbido sufre un rápido metabolismo y por tanto, incide poco sobre la concentración sanguínea. Diversos factores dietéticos pueden modificar la excreción urinaria de citratos que se halla regulada por el equilibrio ácido-base. Éste interviene y regula la cantidad de citrato reabsorbido por la célula y aumenta o disminuye su metabolismo intracelular. La absorción intestinal neta de álcali, una anómala absorción gastrointestinal de citrato, la ingesta de sodio y la dieta hiperproteica son varios de los factores que regulan, de forma indirecta, los niveles de citraturia. La llamada hipocitraturia idiopática ha sido atribuida a estos factores, así como a la presencia de infecciones urinarias de repetición y al ejercicio físico excesivo30.
En 1989 M.OH describe un método sencillo y seguro que permite calcular la absorción intestinal neta de álcali31. En esta fórmula la absorción gastrointestinal neta de álcali es igual a la cantidad de los electrolitos urinarios que se excretan en un día. La fórmula urinaria es:
(Na + K + Ca + Mg) - (CI + 1,8P)
en donde todos esos iones son medidos en mEq/día, a excepción del P que se mide en mM/día. El resultado de esta fórmula nos indica la cantidad neta de álcali absorbido. En sujetos normales, la citraturia/día mantiene una correlación positiva con la absorción intestinal de álcali; es decir, al aumentar la absorción intestinal de álcali aumenta de forma paralela la citraturia/día eliminada. Esta correlación entre la citraturia y la absorción intestinal de álcali se mantiene en los pacientes con síndrome diarreico crónico y en litiásicos con anomalías metabólicas, si exceptuamos la acidosis tubular renal, en la que la hipocitraturia es anormalmente baja respecto al álcali absorbido. En la hipocitraturia idiopática la absorción intestinal neta de álcali está disminuida. Ello sugiere que la hipocitraturia idiopática podría tener un origen intestinal que vendría determinado por una hipoabsorción gastrointestinal de álcali1.
Cowley observó una anómala citraturia tras la ingesta oral de citratos en pacientes con litiasis cálcica y sugirió que una disminución de la absorción intestinal del ácido hidroxicarboxílico podría causar la hipocitraturia29.
Estudios de Fegan, tanto en litiásicos como en controles, demostraron que la absorción del citrato era rápida y eficaz en ambos grupos y que alrededor del 95% del citrato que se ingería era absorbido a las tres horas. Parece, por tanto, que en la hipocitraturia esencial no existe una disminución de la absorción intestinal de citrato.
La ingestión de sodio puede modificar la eliminación de citratos urinarios. En sujetos normales el aumento de la ingesta de sodio (de 50 mEq/día a 300 mEq/día) provocó una disminución significativa de la citraturia (de 593 mg/día a 473 mg/día). Durante el experimento se produjo un descenso del bicarbonato plasmático y una elevación del Cl sanguíneo y del pH urinario. Probablemente esta acidosis metabólica moderada facilita la reabsorción tubular del citrato y su proceso oxidativo intracelular con la consiguiente disminución del citrato urinario32.
Es conocido también que dietas ricas en proteínas animales se asocian con valores bajos de citraturia. N. Breslau halló una correlación inversa entre el aumento de la ingesta de proteínas y el descenso de la citraturia33. Recientemente R. Duran ha confirmado estos datos en la litiasis cálcica y F Grases34, en un modelo experimental con ratas, observa que la dieta hiperproteica facilita la nucleación heterogénea del ácido úrico y que con una dieta controlada, el efecto inhibitorio del citrato y el magnesio era más favorable respecto a dietas con exceso de lípidos, hidratos de carbono o proteínas.
Riñón y citrato
Al efectuar, en animales de experimentación, una nefrectomía, se produce un ascenso de las concentraciones plasmáticas de citrato. Esto indica la importancia de los riñones en el metabolismo y excreción urinaria del citrato. El citrato libre es filtrado por el glomérulo y, en humanos, del 65% al 90% del citrato filtrado es reabsorbido por las células tubulares.
Aproximadamente las tres cuartas partes del citrato filtrado por minuto son reabsorbidas en el túbulo proximal y una cuarta parte se pierde por la orina (Fig. 11.1). Los estudios efectuados (stop flow y perfusión de segmentos tubulares aislados) muestran que el citrato es reabsorbido en el túbulo contorneado proximal y el segmento proximal del túbulo recto, mientras que no se observa reabsorción de citrato en la rama ascendente del asa de Henle ni en el túbulo colector13,35,37
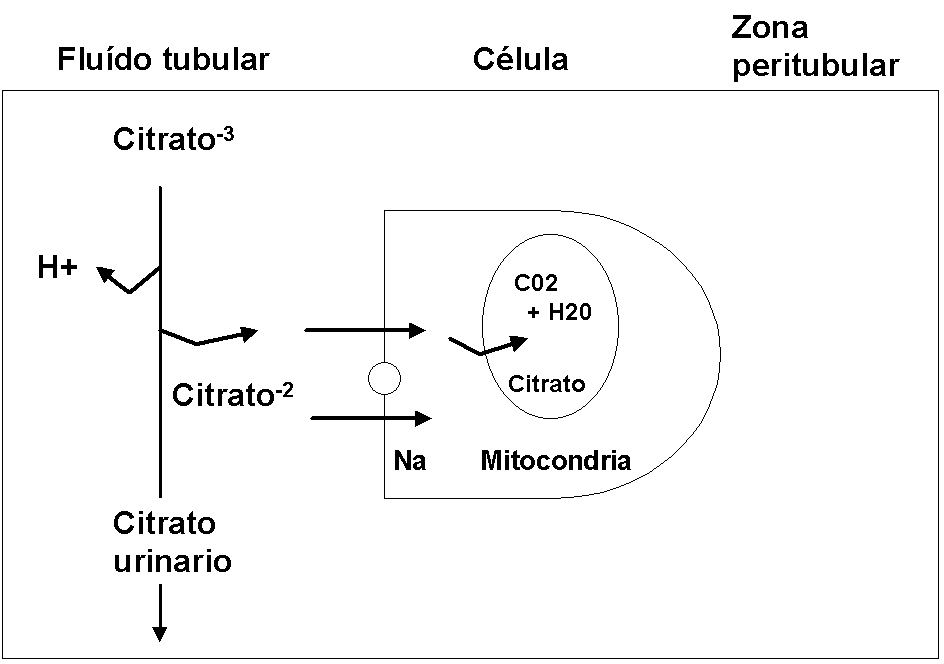
Figura 11.1
Las tres cuartas partes del citrato filtrado son reabsorbidas en el túbulo proximal y una cuarta parte se pierde por la orina
Wright38 ha estudiado la reabsorción del citrato en el túbulo proximal con vesículas de conejo y muestra que la cantidad de citrato transportado es superior a la de los azúcares y aminoácidos. La mayoría de datos disponibles indican que el citrato es transportado como anión divalente (citrato-2), es dependiente del sodio y su carga eléctrica positiva favorece su entrada en la célula.
La forma trivalente (citrato-3) actúa como un competidor-inhibidor del transporte de anión divalente (citrato-2). La oubaína puede bloquear el 80% del citrato reabsorbido y, por tanto, el resto del citrato puede ser transportado a través de un mecanismo pasivo que facilita la permeabilidad de citrato. Por otra parte, la cantidad de citrato reabsorbido en la perfusión del túbulo proximal puede ser superior al citrato que se filtra. En el túbulo contorneado proximal aislado se ha demostrado que la reabsorción del citrato es un proceso unidireccional13,36
Con alfa-cetoglutarato marcado se ha analizado el transporte del citrato en el túbulo. Tiene el mismo transportador que el dicarboxilato, es dependiente del sodio (en el 80%) y el aumento del pH es capaz de disminuir su entrada en la célula39. Algunos autores han postulado la existencia de una secreción urinaria de citrato en la porción distal del túbulo proximal. Con precursores de citrato marcados con C-14 se ha observado su secreción tubular, así como la de dicarboxilato, en ratas. Sin embargo, otros autores no han sido capaces de evidenciar la secreción tubular del citrato. La secreción de citrato tampoco se ha demostrado con la perfusión del mismo en el túbulo contoneado proximal del conejo25
El citrato reabsorbido es metabolizado en la célula tubular. Las células tubulares proximales extraen el citrato de los vasos postglomerulares y del fluido peritubular. La consiguiente oxidación del citrato a dióxido de carbono y agua por la vía del ciclo del ácido cítrico en la mitocondria de las células tubulares, proporciona una importante fuente de energía para el riñón.
En condiciones aerobias se produce la descarboxilación oxidativa a partir del piruvato para formar acetil-CoA y C02. El acetil-CoA se inserta en el ciclo tricarboxílico y reacciona con el oxalacetato para producir citrato y CoA. El citrato sufre una descarboxilación oxidativa y posteriormente el isocitrato se descarboxila, formándose el alfa-cetoglutarato que es catalizado por el complejo alfa-cetoglutarato deshidrogenasa a succinil-CoA. La etapa final del ciclo del ácido cítrico lleva consigo la regeneración del oxalacetato por oxidación del succinato25,35
Factores que regulan la excreción renal de citratos
El equilibrio ácido-base altera profundamente la eliminación del citrato urinario. La acidosis metabólica facilita la entrada del citrato en la célula y aumenta su proceso oxidativo en la mitocondria. Al mismo tiempo se produce un aumento del citrato que se capta del líquido peritubular. El incremento de la oxidación mitocondrial del citrato provoca la disminución del citrato del córtex y la hiperabsorción de citrato, y su ulterior proceso oxidativo da lugar a una disminución del citrato urinario.
El proceso contrario ocurre con la alcalosis. Existe una menor reabsorción tubular de citrato y una reducción del mismo en la mitocondria. Consecuentemente hay, en la alcalosis, un aumento del citrato urinario al disminuir la reabsorción tubular del anión y su proceso oxidativo intracelular.
Estos efectos de la acidosis y la alcalosis sobre la excreción urinaria han sido demostrados en numerosos experimentos. La alcalosis sistemática aumenta el pH intracelular y la concentración de bicarbonato inhibe la oxidación del citrato al disminuir la entrada de éste en la mitocondria.
El aumento de la concentración intracelular de citrato da lugar a una disminución del gradiente entre el citrato intracelular y el intraluminal, que provoca el descenso en la reabsorción tubular de este anión y aumenta su pérdida urinaria. Además del efecto metabólico de la alcalosis sobre la mitocondria, el aumento del pH en el fluido tubular provoca una disminución del citrato-2 que facilita su pérdida urinaria13,25,41-43. Estos dos mecanismos sincrónicos que se observan con la alcalosis son esquematizados en la Fig. 11.2. Con la acidosis ocurren efectos contrarios.
Figura 11.2
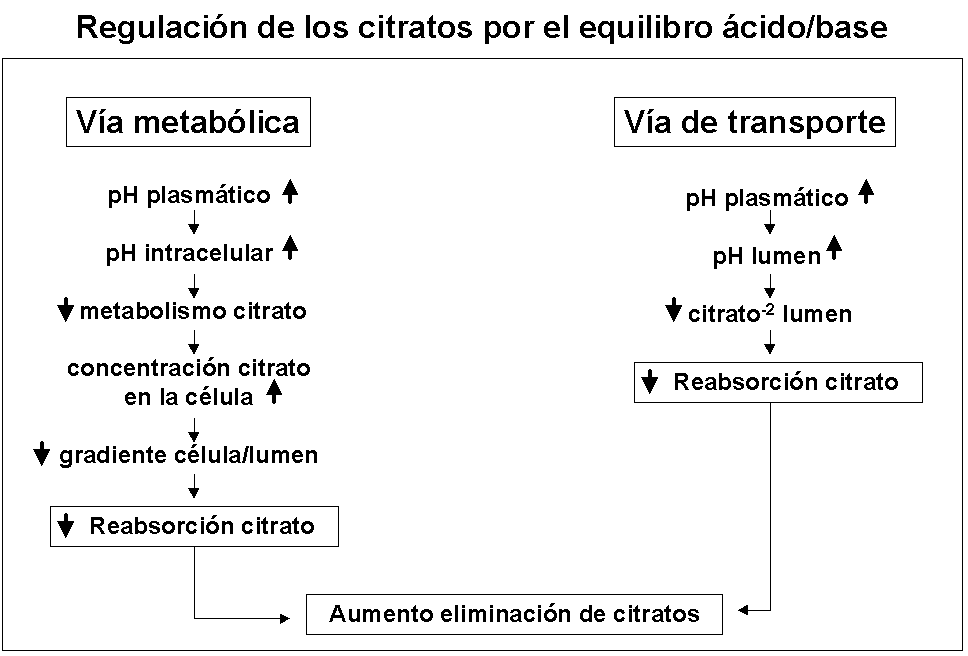
La alcalosis disminuye la reabsorción tubular del citrato y el proceso oxidativo del citrato en la mitocondria. Estas dos vías provocan un aumento de los citratos urinarios. El efecto contrario se produce en la acidosis metabólica.
La hipopotasemia puede dar lugar a una acidosis metabólica en el córtex renal y ésta provoca un descenso en la eliminación de citratos urinarios42. Los ácidos orgánicos (malarato, succinato, fumarato) estimulan la síntesis intrarrenal de citratos y aumentan su excreción urinaria. Ello se debe al efecto alcalino que se obtiene con el aumento de la síntesis de citratos. Varias hormonas alteran también la eliminación de citratos. El citrato aumenta en la última fase del ciclo menstrual y de manera especial durante la gestación. La citraturia es más elevada en mujeres que en hombres y ello está relacionado con la actividad estrogénica. La progesterona tiene un efecto hipocitratúrico45.
La vitamina D, la calcitonina y la parathormona aumentan la excreción de citratos urinarios. Existe una clara relación entre la vitamina D y la citraturia. Dietas con alto contenido en vitamina D elevan la citraturia. La vitamina D disminuye la oxidación del citrato o impide la entrada de éste al interior de la mitocondria46.
La parathormona reduce la eliminación urinaria de citratos al provocar una acidosis metabólica47,48. Sin embargo, en el hiperparatiroidismo primario, con litiasis renal y ausencia de afectación ósea, se ha descrito una marcada hipocitraturia. Probablemente ello se deba a que no existe una movilización de los depósitos óseos de citrato en esta entidad49,50
El aumento del volumen extracelular, la acetazolamida y el ácido etacrínico reducen la concentración de citratos urinarios. En el primer caso se produce una disminución del bicarbonato plasmático y los diuréticos dan lugar a una acidosis metabólica sistémica25,51,52
El plomo y las sales de litio aumentan la citraturia al interferir la reabsorción de citratos en el túbulo proximal1-13
En síntesis, la regulación de la citraturia depende del equilibrio ácido-base. La alcalosis metabólica incrementa la citraturia, mientras que la acidosis la disminuye. Otros factores intervienen de forma secundaria en su excreción urinaria. La infección urinaria, la acidosis tubular, el ayuno prolongado y estados de inanición, la hiperoxaluria primaria, el hiperaldosteronismo primario y varias anomalías electrolíticas, como la hipomagnesemia y la hipocalcemia, alteran la eliminación urinaria de citratos. La Tabla 11.I recoge los factores que regulan la excreción de citratos por la orina.
Tabla 11.I
Factores que modifican la excreción urinaria de citratos
|
Aumento de la excreción de citrato |
Disminución de la excreción de citrato |
|
Litio Vitamina D PTH Calcitonina Estrógenos Hormona de crecimiento Proteínas vegetales Ácidos orgánicos |
Ayuno prolongado Ácido etacrínico Andrógenos Proteínas animales Acetazolamida Menstruación Envejecimiento
|
Citratos y hueso
El hueso es el reservorio del citrato. Alrededor del 90% del citrato que contiene el organismo se halla almacenado en el hueso. Vaes y NichoI28 muestran que el 1% del peso óseo corresponde al citrato y que sus depósitos son movilizados por varios factores entre los que intervienen, fundamentalmente, los estrógenos y la parathormona. Por otra parte, el ácido cítrico actúa también en la reabsorción y el remolado óseo por su acción sobre el ion calcio53.
Citratos e hígado
En el hígado los citratos modulan la velocidad de la biosíntesis de los ácidos grasos ya que el cítrico aumenta la actividad de la carboxilasa, que facilita su difusión al citosol54. También interviene en el transporte de la acetil-CoA desde el interior de la mitocondria al citosol, y en la gluconeogénesis el citrato modula la fosfofructocinasa (enzima que regula esta vía).
TRATAMIENTO CON CITRATO POTASICO DE LA LITIASIS RENAL
El efecto terapéutico del citrato potásico se debe al aumento de los citratos urinarios y a su acción alcalinizante. Existe, con el incremento de la citraturia, una inhibición de la cristalización de las sales cálcicas, y la elevación del pH urinario inhibe la cristalización del ácido úrico1,10,15
Con dosis de 60 mEq/día se produce un ascenso de los citratos y del pH urinario. El citrato potásico es casi absorbido en su totalidad. Se oxida y elimina por vía renal como un álcali. Una pequeña parte del citrato absorbido escapa a la oxidación celular y aparece directamente en la orina, contribuyendo al efecto citratúrico del citrato potásico1,21,55
Acidosis tubular renal
El tratamiento con citrato potásico corrige la acidosis metabólica y la hipopotasemia en la acidosis tubular distal. Ello aumenta los citratos urinarios y disminuye la insolubilidad del oxalato cálcico al producirse un descenso del calcio urinario iónico54,55. Esta terapéutica precisa de dosis elevadas, que están en consonancia con la gravedad de la acidosis2. Preminger4 trató un grupo de 11 pacientes con una acidosis tubular distal incompleta con dosis de citrato potásico que oscilaron entre 60 y 80 mEq/día. Cinco dejaron de formar cálculos y los seis restantes disminuyeron la formación de nuevos cálculos respecto al período pretratamiento. Estos datos demuestran una remisión completa de la litiasis en el 45% de los pacientes y una mejoría en el 95% de los casos.
Yamaguchi58 describe en niños con acidosis tubular distal la remisión de la litiasis en 5 de 9 casos seguidos durante un periodo de 10 años. El efecto terapéutico es atribuido a la alcalinización urinaria, mientras que Tunsanga59 sugiere que la depleción potásica puede contribuir a las anomalías que presentan los sujetos con acidosis tubular renal.
Debe obviarse su empleo en la insuficiencia renal grave (aclaramiento de creatinina > 40 ml/min). En la insuficiencia renal moderada el citrato potásico se asocia a una estricta monitorización del potasio plasmático1-4
Síndrome diarreico crónico
En pacientes con pérdidas de moderadas a importantes de fluido intestinal existe hipocitraturia (100-200 mg/día)
En general, se utiliza la forma líquida en tres o cuatro tomas. Las tabletas, debido a la lenta difusión del citrato y al rápido tránsito intestinal, son poco eficaces60. Por otra parte, la adhesión de las cápsulas a la pared intestinal puede desencadenar obstrucciones intestinales. En hipocitraturias importantes (>l00 mg/día) la terapéutica, aun a dosis altas, no logra restaurar los valores normales de citratos. En el estudio de Dallas6, once pacientes con síndrome diarreico crónico y una actividad de la litiasis muy agresiva (9-10 cálculos/año/paciente) fueron tratados con citrato potásico, obteniéndose una remisión completa en el 54% de los casos y una reducción de la formación de cálculos durante el período terapéutico del 91%. Esta terapéutica precisa de medidas adicionales; la ingesta abundante de líquidos es imprescindible2,6,60
Hipocitraturia secundaria a tiazidas
El tratamiento continuado con tiazidas puede provocar una hipopotasemia asociada a una acidosis intracelular que da lugar a una hipocitraturia. Pacientes con hipercalciuria tratados con diuréticos tiazídicos pueden continuar formando cálculos a pesar de la normalización de la calciuria. Nicar3 emplea citrato potásico a dosis bajas (20-40 mEq/día) para corregir la hipopotasemia-hipocitraturia desencadenada por las tiazidas61. En el estudio de Pak, en 10 pacientes que habían recibido tiazidas, con un rango de formación de cálculos entre 1,3 y 3,5/año, el citrato potásico logró solucionar la recivida calculosa en el 72% de los casos y se obtuvo una reducción individual en el 94%6.
En realidad, la formación de cálculos por año y paciente se redujo de 4,9 durante el periodo pretratamiento a 0,7 cálculos/año/paciente.
Litiasis oxalato cálcica en pacientes con hiperuricosuria
El aumento del urato monosódico incrementa la cristalización del oxalato cálcico. Al añadir citrato en un medio supersaturado respecto al oxalato cálcico se inhibe la nucleación heterogénea del oxalato cálcico provocada por el urato monosódico62.
Pak y Peterson64 muestran los efectos beneficiosos del citrato potásico en 19 pacientes con hiperuricosuria y cálculos de oxalato cálcico. Durante la terapéutica se produjo un ascenso del pH y del citrato urinario, y la formación de cálculos descendió de 1,5 cálculos/paciente/año a 0,4 cálculos/paciente/año durante el periodo de seguimiento terapéutico (2,5 a 3 años). En 16 pacientes la actividad litiásica cesó con unas dosis de citrato potásico que oscilaron entre 60 y 80 mEq/día.
Hipocitraturia idiopática y litiasis cálcica
En este grupo se incluyeron 17 pacientes que presentaban como única alteración hipocitraturia y cálculos renales de oxalato cálcico. Fueron tratados con unas dosis medias de 60 mEq/día de citrato potásico y controlados durante un periodo medio de 3,5 años. La mayoría de los pacientes (85%) no formaron nuevos cálculos durante el periodo de tratamiento y el 97% redujeron significativamente la expulsión o formación de nuevos cálculos respecto al periodo pretratamiento. La asociación de hipocitraturia con hipercalciura en pacientes litiásicos recidivantes y tratados con citrato potásico y diuréticos tiazídicos tiene unos resultados similares a los obtenidos en los pacientes con hipocitraturia aislada.
En ambos estudios se comprobó un ascenso de los citratos, del pH y del potasio urinarios durante el periodo terapéutico2,3,6.
Martini et al. analizan la excreción de calcio y citrato en un grupo de litiásicos y controles en relación al consumo de alimentos ricos en K, así como los factores de riesgo litiásico 63
Estudio aleatorizado a doble ciego con citrato potásico y placebo en la litiasis cálcica hipocitratúrica
Las series publicadas ponen de manifiesto que la terapéutica con citrato potásico mejora de forma ostensible la actividad de la litiasis que presentan estos pacientes. La formación de cálculos por paciente y año varió de 6,2 cálculos/paciente/año durante el periodo pretratamiento a 0,6-0,2 cálculos/paciente/año durante el periodo terapéutico, y la formación individual de cálculos disminuyó en el 90% de los casos, con una remisión completa en el 68% a 82% de los pacientes tratados. Todos estos datos muestran una favorable respuesta terapéutica con citrato potásico en la mayoría de los pacientes. Sin embargo, muchas de estas series comparan la respuesta terapéutica con el periodo pretratamiento64
Diversos autores creen que esta respuesta favorable puede ser atribuida a las medidas dietéticas prescritas (clinic effect stone). Para valorar la eficacia del citrato potásico hemos diseñado un estudio en el que se compara el citrato potásico con un placebo67. Para ello se escogieron 57 pacientes con hipocitraturia aislada y moderada a importante actividad de su litiasis renal. Los pacientes fueron divididos en dos grupos aleatoriamente. El primer grupo fue tratado con una media de 45 mEq/día de citrato potásico y el segundo se trató con tabletas de placebo de idéntica apariencia. Ambos recibieron las mismas indicaciones: aumento de la ingesta de líquidos y reducción de la sal. Los resultados del tratamiento quedan reflejados en las figuras 11.3 y 11.4. Dado que ambos grupos tenían características semejantes en cuanto a su actividad litiásica (1,2 ± 0,6 cálculos/paciente/año versus 1,1 ± 0,4 cálculos/paciente/año) y a sus cifras de citraturia pretratamiento (1,9 ± 0,5 mmol/día versus 1,84 ± 0,7 mmol/día), se pudo comparar el efecto del citrato versus placebo. Los 18 pacientes que finalizaron los 36 meses de tratamiento con citrato potásico formaron 7 cálculos, mientras que los 20 que recibieron placebo formaron 52 nuevos cálculos durante el período de seguimiento, que fue de 36 meses. La formación de cálculos/paciente/año disminuyó de 1,2 ± 0,6 a 0,1 ± 0,2 en los tratados con citrato potásico. Por contra, los tratados con placebo continuaron con la misma actividad (1,1 ± 0,4 a 1,1 ± 0,3). Esta diferencia de resultados y, específicamente, la mejoría obtenida en el grupo tratado con citrato potásico, no puede atribuirse al stone clinic effects dado que las medidas conservadoras fueron idénticas para ambos grupos.
Resultados del tratamiento con citrato potásico (30-60 mEq/día) en la actividad de la litiasis. Cada línea representa un paciente y cada círculo la formación de un nuevo cálculo. Se formaron 58 cálculos en 18 pacientes durante el período de pretratamiento, mientras que durante el período de tratamiento los 18 pacientes formaron 7 cálculos.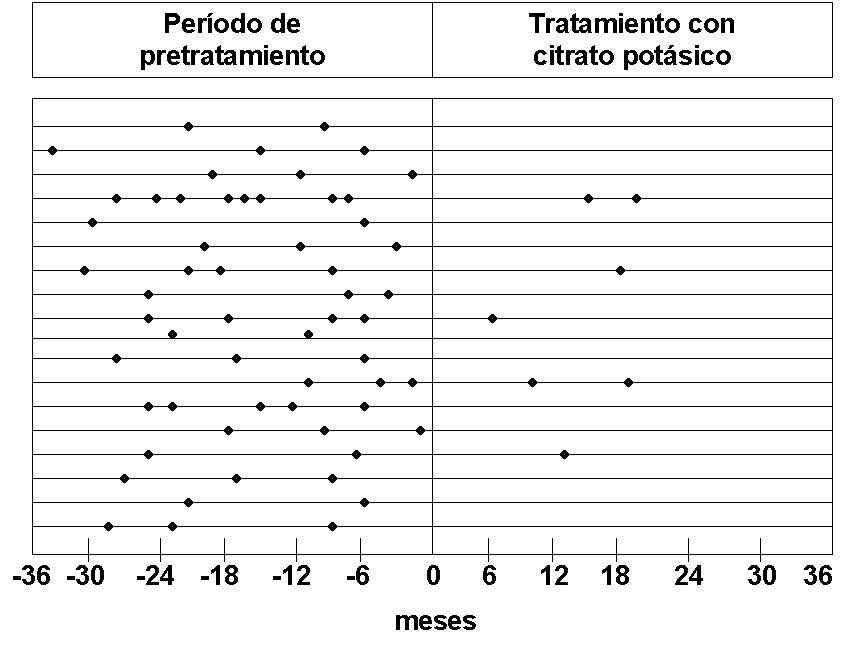
Figura 11.3
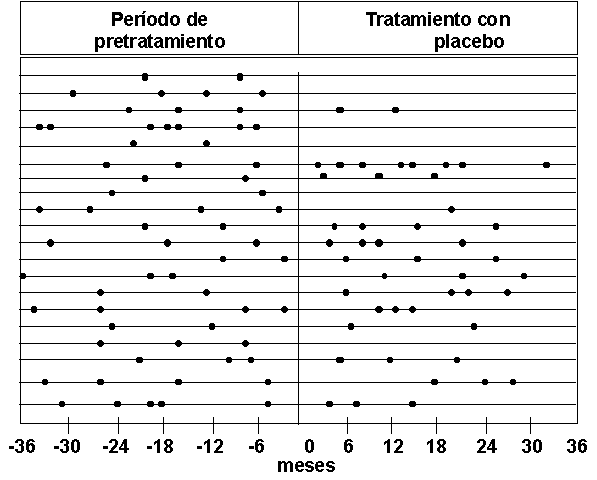
Figura 11.4
Resultados del tratamiento con placebo (6-12 tabletas/día) en la actividad de la litiasis. 20 pacientes formaron 62 cálculos durante el período de pretratamiento y 52 cálculos cuando recibieron placebo.
La respuesta clínica se asoció con un aumento del citrato urinario, del pH y del potasio, sin que se modificaran estos parámetros en los pacientes que tornaban placebo (Tabla 11.II). En conclusión, este estudio confirma la eficacia del citrato potásico, que es capaz de inhibir la formación de cálculos cálcicos en pacientes con hipocitraturia67
Tabla 11.II
Acciones fisiológicas del citrato potásico (grupo tratado con citrato potásico)
|
|
Citrato nmol/día |
pH urinario |
Potasio mEq/día |
|
Pretratamiento |
1.9±0.5 |
5.4±0.5 |
61±17 |
|
Tratamiento 3 meses 6 meses 12 meses 18 meses 24 meses 30 meses 36 meses |
3.0±0.4* 3.1±0.5* 2.8±0.8* 3.4±0.3* 3.2±0.5* 3.5±0.5* 3.3±0.5* |
6.3±0.7* 6.5±0.5* 6.1.±0.6* 6.7±0.4* 6.5±0.5* 6.6±0.4* 6.4±0.3* |
86±26* 93±45* 83±31* 102±37* 98±40* 115±47* 105±41* |
|
* p<0.01 respecto a los valores pretratamiento |
|||
Recientemente se ha efectuado un análisis del coste efectividad del tratamiento preventivo de la litiasis cálcica, empleando citrato potásico versus terapéutica con dieta y líquidos. Este estudio demuestra la eficacia del citrato potásico, sea cual sea la forma de su ingesta.
Expulsión de fragmentos calculosos postlitotricia
Los efectos fisiológicos del citrato potásico sobre la solubilidad urinaria han propiciado su empleo en la expulsión de los fragmentos calculosos postlitotricia. En un estudio efectuado por nosotros (datos no publicados) se observó una mejora significativa en la expulsión de fragmentos calculosos en los pacientes que recibieron citrato potásico (30 mEq/día) frente a los tratados con las normas habituales. Resultados similares sobre el empleo del citrato potásico en la postlitotricia se han publicado recientemente30,71
EFICACIA DEL CITRATO POTÁSICO COMPARADO CON OTROS ALCALINIZANTES
La eficacia de este fármaco se valora en relación a los cambios urinarios provocados por su empleo, por la capacidad de frenar la evolución de la actividad de la litiasis y por sus efectos indeseables.
Jarabe de citrato potásico en comparación con wax matrik
En el estudio de Dallas, 84 pacientes fueron tratados con citrato potásico en forma líquida y 100 con tabletas (WMCP). Los efectos fisiológicos de ambos preparados fueron idénticos; sin embargo, el grado de tolerancia digestiva fue muy superior con la WMCP que con la poción citratada. Desde 1985 la WMCP se ha universalizado, mientras que la forma líquida es prácticamente apartada de la farmacopea y su única indicación queda relegada al síndrome diarreico crónico 2,6,72
Citrato potásico versus sales de sodio
El citrato potásico es superior al citrato sódico en los incrementos que se producen de los citratos urinarios. Las sales de sodio, en algunos casos, producen un aumento del calcio urinario; sin embargo, el citrato potásico disminuye la calciuria en la acidosis tubular renal y lo disminuye o no lo altera de forma significativa en otras patologías. En la prevención de los cálculos cálcicos el citrato potásico es más eficaz que el citrato sódico. Ambos mantienen una eficacia similar en el tratamiento de la litiasis úrica
Citrato potásico versus zumo de naranja
El zumo de naranja es idéntico a una preparación líquida que contiene citrato potásico y ácido cítrico. Ambos producen un aumento similar del pH urinario y de los citratos. El zumo de naranja provoca un aumento del oxálico urinario, sin alterar la calciuria. Un efecto contrario se observa con el citrato potásico: no modifica la oxaluria y puede disminuir el calcio urinario. Estos datos muestran que el zumo de naranja no reduce la saturación urinaria del oxalato cálcico72,76. Rousaud ha demostrado que la cantidad de zumo (naranjas) que debe ingerirse para unas dosis medias-altas son difícilmente aplicables en un tratamiento continuado y, por otra parte, su coste es más elevado que el del citrato potásico (datos no publicados).
Efectos indeseables
La tolerancia digestiva del citrato potásico es la norma; sólo la preparación líquida provoca molestias gastrointestinales: náuseas, dolor epigástrico o distensión abdominal. Estos efectos secundarios quedan minimizados si el citrato potásico se ingiere después de las comidas. Las erosiones gástricas, así como la oclusión intestinal, son posibles, aunque no han sido publicadas con la WMCP 2,72
En nuestro estudio la tolerancia digestiva del citrato potásico fue similar a la del placebo y no hubo cambios significativos en el calcio, fósforo, creatinina, sodio, potasio, cloro, C02, ácido úrico y hematocrito durante el periodo de tratamiento 67
En los pacientes en que se asocia una terapéutica con diuréticos ahorradores de potasio deben ajustarse particularmente las dosis y monitorizar cuidadosamente la concentración sérica de potasio 2, 72
Se ha descrito que en sujetos mantenidos con una dieta proteica elevada se produce un aumento de la absorción intestinal de calcio. Esta hiperabsorción cálcica se produce sin que haya modificaciones en los niveles séricos de vitamina D1,25(OH)277. Puede coexistir una hiperabsorción de aluminio durante la terapéutica con citrato potásico; sin embargo, el aluminio sérico no modifica su concentración por el aumento del aluminio urinario. Sólo en la insuficiencia renal moderada-avanzada, el acúmulo óseo de aluminio aumenta 78, 79
BIBLIOGRAFIA