"RELEVANCIA DE LOS NIVELES DE 25 HIDROXIVITAMINA D EN PACIENTES CON INSUFICIENCIA RENAL CRONICA"
C. Gómez Alonso, J B. Cannata Andía
Servicio de Metabolismo Óseo y Mineral.
Instituto Reina Sofía de Investigación. Hospital Universitario Central de Asturias
Oviedo. Espańa
cgomez@hca.es, cannata@hca.es
Sistema hormonal de la vitamina D
La vitamina D es una hormona sistémica que actúa en diversos órganos diana, entre los que destacan intestino, rińón, paratiroides, hueso y sistema inmunitario. Su principal objetivo es, junto con la PTH, regular la homeostasis mineral, fundamentalmente de calcio y fósforo. Los efectos de la vitamina D van a depender del tipo de metabolito, de los niveles circulantes, de la densidad de receptores (regulados al alza por la propia vitamina D) y posiblemente de aspectos cualitativos de los propios receptores (Figura 1) 1.
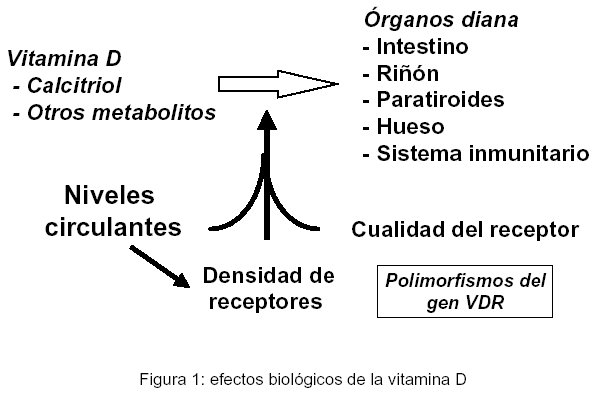
Los diferentes metabolitos que conforman el sistema hormonal de la vitamina D incluyen desde precursores de síntesis cutánea o componentes dietéticos, hasta el metabolito más activo, la 1-25 hidroxivitamina D o calcitriol. Pese a ser el calcitriol quien va a actuar fundamentalmente sobre los receptores de los órganos diana, el metabolito que se reconoce como el mejor indicador del estado de los depósitos o "status" de la vitamina D es la concentración de 25-hidroxivitamina D 2.
El calcitriol se sintetiza fundamentalmente en el rińón, por acción de la 1-alfahidroxilasa sobre la 25-hidroxivitamina D. La actividad de la 1-alfahidroxilasa está regulada por la PTH (estimulada) y por los niveles de fósforo (inhibida). A medida que disminuye la función renal decrece la capacidad de sintetizar calcitriol, que secundariamente altera la capacidad de absorción intestinal de calcio y esta tendencia a la hipocalcemia estimula la liberación de PTH (que estimula la actividad 1-alfahidroxilasa) y promueve la resorción ósea para mantener la calcemia en límites normales. La progresión de la IRC disminuye la capacidad de eliminación de fósforo cuyo acúmulo inhibe la actividad de la 1-alfahidroxilasa y estimula la liberación de PTH conformando el hiperparatiroidismo secundario característico de la IRC 3. Resaltar que éste no es sino un intento de mantener la homeostasis del calcio, si bien finalmente va a tener consecuencias negativas esqueléticas y extraesqueléticas.
Vitamina D e IRC
Los mecanismos fisiopatológicos implicados en la génesis del hiperparatiroidismo secundario en pacientes con insuficiencia renal crónica (disminución de calcemia, aumento de fosforemia, alteraciones en receptor del calcio, disminución de calcitriol, disminución de receptores de vitamina D, acidosis, toxinas urémicas, desarrollo de resistencia esquelética a la PTH e inducción de hiperplasia nodular) 4 son tan variados y de tanto peso que pudiera parecer irrelevante la participación de los niveles de 25-hidroxivitamina D en este contexto.
Sin embargo, la importancia real de los niveles de 25-hidroxivitamina D en pacientes con insuficiencia renal crónica está condicionada por cuatro aspectos 5
- La 25-hidroxivitamina D es el sustrato del calcitriol y, aunque en circunstancias normales la actividad 1-alfahidroxilasa no sea sustrato dependiente, en la insuficiencia renal crónica puede llegar a serlo.
- Tanto el calcitriol como el 25-hidroxicolecalciferol son capaces de unirse y activar el receptor de vitamina D. La afinidad es muy superior para el calcitriol (1:2400) pero la relación de concentraciones es favorable para el 25-hidroxicolecalciferol (1000:1).
- Algunas acciones de la vitamina D, como la absorción intestinal de calcio, son acciones no genómicas, con un ratio de potencia de 1:8
- La existencia de 1-alfahidroxilasa extra-renal (sistema monocito/macrófago, células óseas) hace que los niveles de 25-hidroxivitamina D circulantes puedan tener relevancia como un factor local paracrino.
Quizá por ello se expliquen los resultados de un estudio en 113 pacientes en hemodiálisis, en los que se observaron diferencias en el patrón radiológico (zonas de resorción y líneas de Looser) en los pacientes con valores más bajos de 25-hidroxivitamina D, sin existir diferencias en los niveles de calcitriol 6. La correlación entre los valores de PTH y 25-hidroxivitamina D observada en este grupo de pacientes fue idéntica a la encontrada en 87 pacientes con trasplante renal enviados sucesivamente a nuestro servicio para valorar la afectación ósea 7 y, a la observada en nuestra población general 3, auque se mueven en diferentes niveles de PTH condicionado por los factores particulares que induce la uremia (Figura 2).
Valores deseables de 25 hidroxivitamina D
Es importante seńalar que la definición de deficiencia de vitamina D y normalidad o estatus adecuado de la misma no ha alcanzado un consenso definitivo. Pero si hasta fechas recientes se aceptaba que valores de 25-hidroxivitamina D por debajo de 5-7 ng/ml inducen osteomalacia, valores inferiores a 10-12 ng/ml condicionan hiperparatiroidismo secundario y osteoporosis y, se consideraban normales niveles superiores a 18-20 ng/ml 8, 9 hoy en día se ha constatado la inadecuación entre los valores derivados de criterios de normalidad establecidos con población joven y la realidad observada cuando se aplican a personas de edad avanzada o enfermos, en los que con esos criterios de normalidad la prevalencia de hiperparatiroidismo es muy elevada, y ha llevado a proponer una clasificación menos conservadora que define como "deseable" unos niveles >40 ng/ml o >100 nmol/l, hipovitaminosis D cuando la concentración se sitúa entre 20 y 40 ng/ml o 50-100 nmol/l, insuficiencia de vitamina D para concentraciones entre 10-20 ng/ml o 25-50 nmol/l y deficiencia de vitamina D para valores inferiores a 10 ng/ml o 25 nmol/l 10, 11. Con estos criterios apenas un 10% de la población por encima de 50 ańos tiene valores de 25-hidroxivitamina D en el rango deseable 11.
Si la larga vida media de la 25-hidroxivitamina D (y la posibilidad de hipercalcemia de difícil manejo en caso de sobredosificación) y su utilización a altas dosis en el pasado hicieron desplazar el tratamiento con vitamina D a metabolitos más activos (calcitriol, 1-alfavitaminaD) 3 los nuevos datos disponibles hacen aconsejable replantearse la necesidad de mantener unos niveles deseables de 25-hidroxivitamina D desde fases incipientes de la insuficiencia renal crónica.
Conclusión
Los niveles 25-hidroxivitamina D más apropiados o deseables para nuestra población en riesgo de padecer enfermedades metabólicas óseas deberían ser superiores a 30 ng/ml. Si bien en la decisión de tratar o no a un determinado paciente se deben tomar en cuenta otros factores, no podemos olvidar que la prevalencia de hipovitaminosis D en población general, en IRC en hemodiálisis o en el postrasplante renal, utilizando dicho punto de corte se sitúa en el 90%. Alcanzar 30 ng/ml es hoy día considerado clínicamente adecuado y seguro para el manejo de la pacientes con riesgo de desarrollar alteraciones metabólicas óseas y/o hiperparatiroidismo secundario 12.
Bibliografía
1.- Gómez Alonso C, Naves ML, Fernández Martín JL, Diaz Corte C, Cannata JB. Metabolismo óseo y polimorfismo del gen del receptor de la vitamina D. Bases fisiopatológicas y datos de la población general. Nefrología 2001, supl 1: 45-50.
2.- McKenna MJ. Differences in vitamin D status between countries in young adults and the elderly. Am J Med 93: 69-77, 1992
3.- Cannata-Andía JB, Gómez Alonso C. Vitamin D deficiency: a neglected aspect of disturbed calcium metabolism in renal failure. Nephrol Dial Transpl 17: 1-4, 2002
4.- Cunningham J, Makin H. How important is vitamin D deficiency in uraemia? Nephrol Dial Transplant. 12:16-8, 1997
5.- Fournier A, Fardellone P, Achard JM, Ghazali A, Pruna A, El Esper N, Moriniere P. Importance of vitamin D repletion in uraemia. Nephrol Dial Transplant. 14:819-23, 1999.
6.- Ghazali A, Fardellone P, Pruna A, et al. Is low plasma 25-(OH)vitamin D a major risk factor for hyperparathyroidism and Looser's zones independent of calcitriol? Kidney Int. 55: 2169-2177, 1999.
7.-Gómez Alonso C, Naves Díaz ML, Rodríguez García M, Fernández Martín JL, Cannata Andía JB. Revisión del concepto de suficiencia e insuficiencia de vitamina D. Nefrología 2003; supl 2: 73-77.
8.- Ringe JD. Vitamin D Deficiency and Osteopathies. Osteoporos Int. 8:S35-S39, 1998.
9.- Vieth R. Vitamin D supplementation, 25-hydroxyvitamin D concentrations, and safety. Am J Clin Nutr. 69:842-56, 1999
10.- McKenna MJ, Freaney R. Secondary Hyperparathyroidism in the Elderly: Means to Defining Hypovitaminosis D. Osteoporos Int. 8:S3-S6, 1998
11.- Gómez Alonso C, Naves Díaz ML, Fernández Martín JL, Díaz López JB, Fernández Coto MT, Cannata Andía JB. Vitamin D status and secondaryb hyperparathyroidism: the importance of 25-hydroxyvitamin D cut-off levels. Kidney Int 2003; supl 85: s44-s48.
12.- Heaney RP. Vitamin D: How much do we need, and how much is too much?. Osteoporos Int. 11:553-555, 2000.
| 