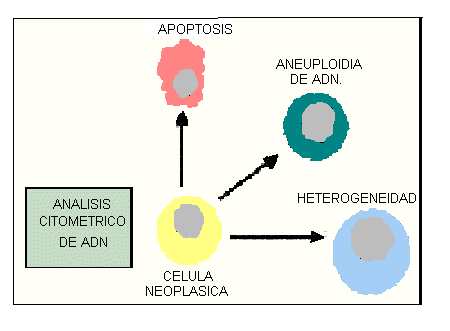
Fig 1. Información proporcionada por el análisis citométrico del ADN
Dentro de las múltiples aplicaciones de la CF en la práctica
clínica nos vamos a centrar aquí en la contribución del
análisis citométrico del ciclo celular al diagnóstico y manejo
terapéutico de los tumores sólidos. Actualmente, a partir de
este análisis, podemos obtener información a cerca de:

Fig 1. Información proporcionada por el análisis citométrico
del ADN
Los núcleos de las células neoplásicas están sujetos a anormalidades en relación al contenido celular en ADN que se conocen como aneuploidías de ADN. De este modo, un contenido aneuploide de ADN refleja anomalías numéricas o estructurales a nivel cromosómico como consecuencia de la desestabilización genómica. La Citometría de flujo aplicada al estudio de ADN en tumores sólidos nos proporciona información a cerca de la existencia de distintos clones celulares presentes. Las medidas del contenido en ADN deben ser referidas a células referencia con contenido normal en ADN y las diferencias entre ambas deben ser expresadas en términos del INDICE DE ADN. El índice de ADN es la relación entre el valor modal o la media del pico G0/G1 de la población anormal respecto de la moda o la media del pico G0/G1 de la población de referencia.
media o moda del valor de
fluorescencia del pico Go/G1 de la población anormal
ID=
------------------------------------------------------------------------------------------------------
media o moda del valor de
fluorescencia del pico Go/G1 de la población de referencia
El término “aneuploidía de ADN” puede ser utilizado para describir una muestra que contiene una población con un contenido citométrico de ADN anormal, mientras que el término “aneuploidía” se reserva para describir anomalías citogenéticas. Lo mismo es válido para “contenido diploide en ADN” y “diploide”.
La proliferación celular es una característica fundamental
para mantener el estado de homeostasis tisular caracterizado por
un equilibrio entre la producción y la muerte celular. La
cuantificación de la actividad proliferativa y de la cinética
celular es útil en el estudio de este proceso biológico para
estimar el potencial de crecimiento tumoral.
En el estudio de ciclo celular por Citometría de Flujo, el parámetro que cuantifica la actividad proliferativa es el porcentaje de células en fase S, sin embargo es posible cuantificar el resto de fases del ciclo: G0/G1 y G2/M frente a otros marcadores como PCNA, BrdUrd, Ki-67 o el contaje de mitosis (Fig 2).
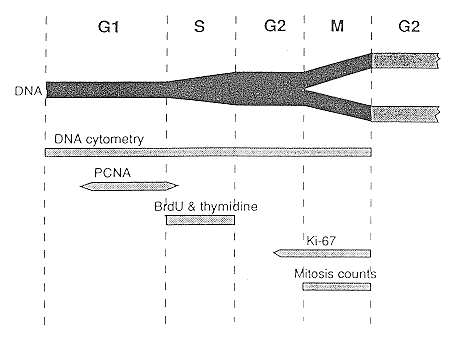 Fig.2
Fig.2
En términos generales los estudios del ciclo
celular generan una información diferente para tumores con
contenido diploide o aneuploide de ADN. Así pues, en aneuploides
hace referencia al porcentaje de células anómalas analizando
estas separadamente de las células diploides (tumorales o no
tumorales). En los tumores diploides la fase S corresponde a la
suma de células normales y tumorales presentes en la muestra.
Algunos autores proponen utilizar los parámetros de dispersión
de la luz frontal y lateral proporcionados por el citómetro para
distinguir poblaciones en función a su tamaño y complejidad.
(Fig 3).
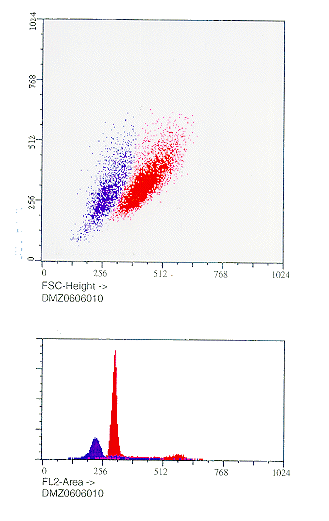 Fig. 3
Fig. 3
Por otra parte se hace necesario establecer distintos puntos de corte en el porcentaje de células en fase S (fase S alta, media o baja) para tumores con contenido en ADN diploide y para los tumores con contenido en ADN aneuploide.
Pool de apoptosis
La mayoría de las células de eucariotas superiores tienen la
capacidad de autodestruirse por activación de un mecanismo
celular de suicidio programado cuando no son necesarias o están
seriamente dañadas. El término apoptosis fue definido
originalmente para incluir ciertas características morfológicas
como daños en la membrana, disminución del tamaño nuclear y
citoplasmático, y condensación de la cromatina diferentes al
proceso de necrosis (Fig 4). Esta definición inicial ha llegado
a ser utilizada ampliamente para referirse a todas las
características morfológicas y bioquímicas de la muerte
celular programada.
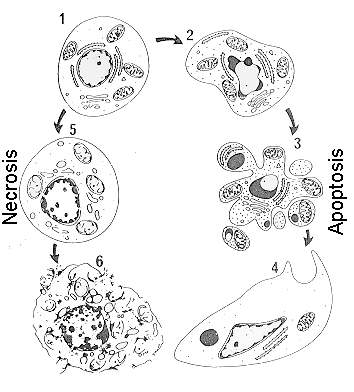 Fig.4
Fig.4
Una característica presente frecuentemente en
las células en apoptosis es la ruptura o escisión del ADN. Este
hecho ha provocado el desarrollo de nuevos ensayos por CF para
identificar y cuantificar el pool de células en apoptosis. En
general existen dos aplicaciones para detectar estas rupturas del
ADN nuclear: la primera está basada en la extracción del ADN de
bajo peso molecular previa a la tinción celular; la segunda, en
el marcaje de estas rupturas del ADN in situ. Cuando se utiliza
la primera aplicación, el contenido en ADN, tras la
permeabilización con detergentes o precipitación con alcoholes,
disminuye y como consecuencia, es detectado como células con
baja tinción para el ADN en el pico “sub-G1”. En la
actualidad existen programas informáticos capaces de analizar
las fases del ciclo celular incluida la población sub-G1. En la
Fig 5 se muestra el pico de apoptosis (Ap).
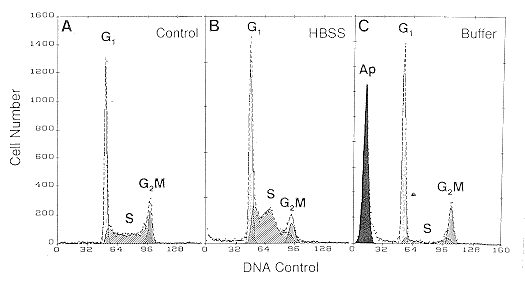 Fig. 5
Fig. 5
Es conocido que la carcinogénesis es un proceso
asociado a cambios genómicos en una célula somática singular
cuya generación y expansión produce subclones anormales. Estos
clones anormales en contenido de ADN son detectados
frecuentemente en lesiones malignas y premalignas con el uso de
la CF. La citometría de ADN proporciona por tanto una
aproximación de los cambios genómicos ocurridos en las células
tumorales.
El análisis de ploidía de ADN ha sido utilizado para investigar
la heterogeneidad tumoral existente tanto en carcinomas primarios
como en metástasis con el fin de aumentar los conocimientos
sobre la biología tumoral en relación a su progresión
(invasión y metástasis) Fig 6.
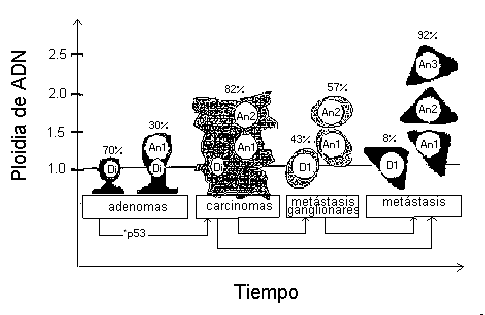 Fig. 6
Fig. 6
A modo de ejemplo se muestran dos histogramas de ADN de un tumor
glótico analizado en nuestro Servicio de Citometría en el que
se detectan distintas aneuploidías en la muestra periférica o
interna del tumor
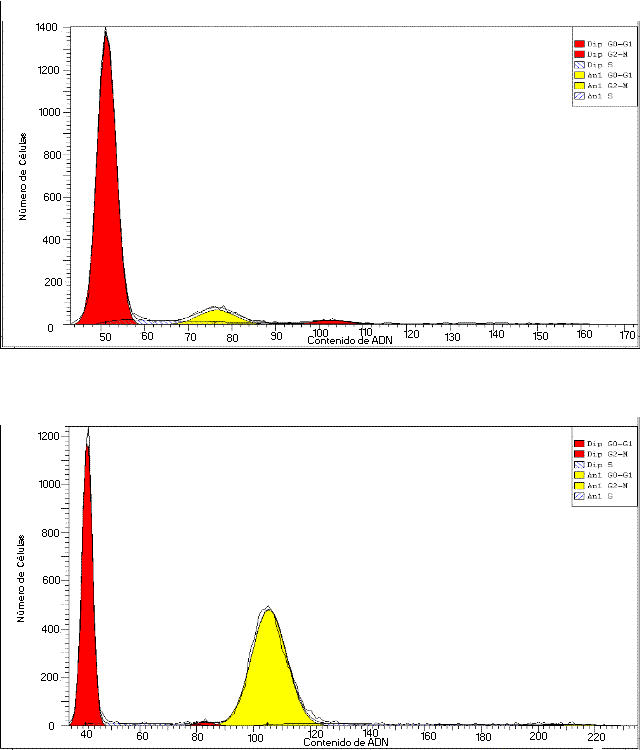 Fig.
7
Fig.
7
El estudio del contenido en ADN, dada la
heterogeneidad regional de muchos tumores primarios, está en
estrecha relación con una buena toma de muestra, cuando esta se
realiza de manera óptima existe un aumento en la detección de
tumores multiploides, es decir con más de una población
aneuploide.Fig 8.
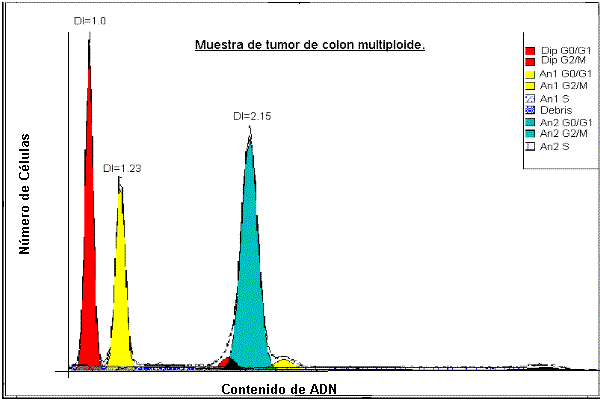
Por otra parte, el estudio de la heterogeneidad por CF puede ser de utilidad para explicar disparidades pronósticas formuladas únicamente en base a parámetros clinico-patológicos.