| Autores: Enrique de Jongh Cobo*; Ramiro Pereira Riverón*; Susana A. Fernández
Benítez*;
Alejandra Barbosa Pastor*; Marieta de la Barrera Fernández**
Institución: * Servicio de Neurocirugía, Hospital Universitario "Gral. Calixto
García".
** Servicio de Anestesiología, Clínica Central "Cira García".
La Habana, Cuba
Email: dejongh@infomed.sld.cu
Resumen
Introducción
Material y Método
Resultados y Discusión
Conclusiones
Bibliografía
Enviar Comentarios
RESUMEN
Las técnicas neuroendoscópicas han incrementado su
desarrollo en la última década y con ello la calidad de vida de los pacientes
intervenidos. Conociendo la necesidad de su introducción como parte de nuestra labor
asistencial, pero sabiendo lo difícil de obtener los equipos en el mercado internacional
por sus altos costos, decidimos buscar e implementar soluciones alternativas. Utilizamos
broncoscopios y artroscopios acoplados a fuentes de luz y cámaras propias de cirugía
laparoscópica y endoluminal con el fin de realizar visualización y tratamiento
neuroquirúrgico bajo visualización endoscópica. Se intervinieron 28 pacientes. Los
procederes realizados fueron: Ventriculostomía premamilar endoscópica en la
hidrocefalia: 24, toma de biopsias: 5, evacuación de quistes tumorales: 3, endoscopía
diagnóstica: 5, y colocación de catéter de derivación ventrículo-peritoneal bajo
visualización endoscópica: 1. Se discuten las ventajas y desventajas de la
neuroendoscopía con soluciones alternativas. Se demuestra la factibilidad de la
generalización de la neuroendoscopía en nuestro país con soluciones alternativas en
hospitales que cuenten con servicios de cirugía endoscópica para otras especialidades.
INTRODUCCION
Aunque la endoscopía intracraneal comenzó su
desarrollo a principios del actual siglo, no fue hasta hace pocos años en que realmente
tomó auge dentro del mundo neuroquirúrgico. Esta técnica de mínimo acceso forma parte
del esfuerzo de muchos cirujanos por causar el menor daño posible a las estructuras
corporales por las que forzozamente tienen que atravesar en sus intervenciones. Su
implementación en la neurocirugía tiene sobrada justificación, teniendo en cuenta la
naturaleza de las estructuras nerviosas que deben ser penetradas durante el acto
quirúrgico.
Los primeros esfuerzos realizados en la endoscopía
neuroquirúrgica se remontan al año 1910 con el empleo de un cistoscopio rígido para
fulgurar el plexo coroides en niños con hidrocefalia (1). Posteriormente, pero de forma
esporádica, se fueron realizando intervenciones neuroendoscópicas con fines
diagnósticos y terapéuticos en el encéfalo y médula espinal utilizando variados
instrumentos (2,3,4,5,6,7,8, 9,10).
En Cuba, alrededor del año 1945, los profesores
Carlos M. Ramírez-Corría y Jesús Meléndez Bergillo emplearon un endoscopio rígido
para electrocoagular el plexo coroides en niños hidrocefálicos, en el Hospital
"Calixto García", Ciudad de La Habana (Meléndez, J.: Comunicación personal ,
1996). En 1956, el Dr. Jorge Picaza, ayudado por el Profesor Rafael Gallardo Carnisé y
otros, utilizaron un endoscopio para Urología Pediátrica y realizaron
electrocoagulación del plexo coroides en niños hidrocefálicos, así como comunicación
del ventrículo lateral con las cisternas peripedunculares (fístula de Hindman). Estos
procederes se realizaban en el Hospital Infantil, Ciudad de La Habana, actual "Pedro
Borrás" (Gallardo, R: Comunicación personal, 1996).
En general el desarrollo de la técnica ha
favorecido el empleo de la neuroendoscopía principalmente con fines diagnósticos. Sin
embargo, en los últimos años la creación de instrumental para el desarrollo de
procederes endoscópicos va permitiendo un incremento de sus aplicaciones con fines
terapéuticos (11).
A finales del año 1994 comenzó a realizarse en el
Centro Internacional de Restauración Neurológica (CIREN) la cirugía endoscópica
intracraneal con neuroendoscopios rígidos y flexibles en diferentes tipos de lesiones
intracraneales (Ochoa, L.: Comunicación personal, 1996). Su implementación en otros
servicios de neurocirugía del país se ha visto frenado por los altos costos del
instrumental en el mercado internacional.
Ante la impetuosa necesidad del desarrollo de
técnicas neuroendoscópicas y la imposibilidad de obtención de equipos convencionales,
en 1996 decidimos comenzar a utilizar broncoscopios y artroscopios, acoplados a cámaras y
fuentes de luz de cirugía general y vías digestivas (endoluminal).
El propósito de este trabajo es demostrar que con
nuestros recursos podemos hacer neuroendoscopía y exponer las ventajas y desventajas de
cada uno de los equipos utilizados. Por otra parte, conociendo que en todos los hospitales
provinciales del país se ha desarrollado la endoscopía para otras especialidades,
queremos demostrar la factibilidad de la generalización de las técnicas
neuroendoscópicas con soluciones alternativas.
MATERIAL
Y METODO
Nuestro centro cuenta con un departamento de
Cirugía Endoscópica (Figura 1). con el que se
ha acordado un convenio de trabajo y nos brinda apoyo: asesoría técnica, facilidades
para uso de sus salones de operaciones, equipos para cirugía laparoscópica y endoluminal
con video, taller para creación y reparación de equipos.
También contamos con:
1-Broncoscopio
flexible (Figuras 2a, 2b y 3): (Olympus)
de 5 mm de diámetro, propiedad del departamento de Anestesia del Instituto de Neurología
y Neurocirugía (INN) con el que se estableció un protocolo de trabajo. Este tiene un
canal de 2 mm de diámetro, pero no tiene canal para irrigación, ni succión. La
irrigación se realiza por el mismo canal de trabajo cuando no se están utilizando otros
instrumentos y la succión se realiza por rebosamiento entre el broncoscopio y el cerebro.
También por el canal de trabajo alternándolo con la irrigación. Se acopla a cámara y
fuente de luz de Xenón para cirugía endoluminal (Figura 4)
2-Artroscopio rígido:
(Karl Storz) de 5 mm de diámetro con canal de irrigación y succión, sin canal de
trabajo, que se acopla a cámara y fuente de luz para cirugía laparoscópica o
artroscópica.
Además, se establecieron protocolos de trabajo
cooperativo con los servicios de neurocirugía de los hospitales Provincial de Pinar del
Río, "Luis Díaz Soto" y "Hermanos Ameijeiras". Se realizaron
intervenciones fuera de nuestro centro utilizando en algunos casos equipos propios de cada
hospital.
La introducción de los endoscopios en el cráneo se
realizó bajo anestesia general orotraqueal y a través de un agujero de trépano o
trefina (de 2 cm de diámetro). El sitio de ubicación del agujero fue preferiblemente del
lado derecho, a 2 cm por delante de la sutura coronal y 3 cm por fuera de la línea media,
en el caso de la hidrocefalia o de lesiones de los ventrículos. Otros sitios de
penetración al cráneo fueron elegidos por los cirujanos según la patología del
paciente. Previo a la introducción de los endoscopios se punciona ventrículo con trócar
de Cushing y por el canal labrado se introduce el mismo.
Selección de pacientes:
Se realizó un trabajo prospectivo y aleatorio que
incluyó mayormente pacientes atendidos en el Servicio de Neurocirugía del Hospital
Universitario "Gral. Calixto García". Se atendieron pacientes de otros
hospitales anteriormente relacionados.
Se incluyeron pacientes con diagnóstico positivo
de:
1-.Hidrocefalia comunicante o no comunicante.
2-.Tumores y quistes intraventriculares o de los
lóbulos cerebrales.
Fueron llevados al quirófano 29 pacientes. Uno de
ellos era portador de un Lupus Eritematoso Sistémico y por consiguiente de una
vasculopatía que produjo intenso sangramiento en todos los planos quirúrgicos desde la
piel. Desde la introducción del trócar de Cushing para localizar el ventrículo se
obtuvo LCR hemorrágico y al visualizar el ventrículo lateral con el endoscopio no se
pudo determinar el sitio indicado para la fenestración por la presencia de numerosos
coágulos. Por todo lo anterior excluimos este caso de nuestra muestra.
RESULTADOS Y DISCUSION
Se intervinieron un total de 28 pacientes (Tabla 1). De ellos, 22 fueron en nuestro centro, 4
pacientes fueron intervenidos en el hospital "Hermanos Ameijeiras", 1 en el
hospital Provincial de Pinar del Río y 1 en la Clínica 43, por el grupo de los autores
en coordinación con especialistas de cada centro.
En 19 de los 21 pacientes intervenidos en nuestro
centro utilizamos el broncoscopio flexible de 5 mm, acoplado a la fuente de luz y a la
cámara de video de equipos de cirugía endoluminal. En los otros 2 pacientes empleamos el
artroscopio rígido de 5 mm acoplado a fuentes de luz y cámara de cirugía
laparoscópica. Para los pacientes intervenidos en el hospital "Hermanos
Ameijeiras" hemos utilizado artroscopios rígidos de las especialidades de Ortopedia
y de Reumatología de dicho centro con similares características técnicas que el que
poseemos (descrito en Material y Método). El paciente intervenido en el hospital
Provincial de Pinar del Río se hizo con el broncoscopio de 5 mm. Para el paciente operado
en la Clínica 43 se contó con un broncoscopio flexible, de 3 mm de diámetro, con canal
de trabajo de 1 mm, sin irrigación ni succión añadidas (estas 2 funciones se realizaron
de igual forma que con el broncoscopio de 5 mm explicado anteriormente). Este broncoscopio
se acopla a cámara y fuente de luz como las utilizadas por Cirugía Laparoscópica.
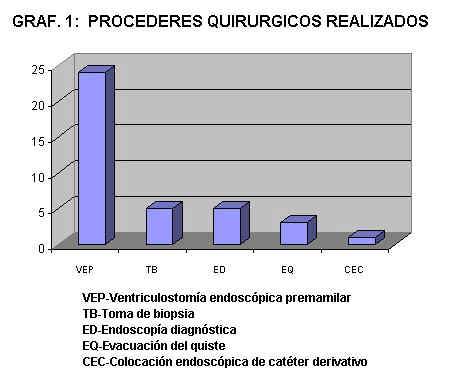
Los procederes neuroendoscópicos realizados fueron:
Ventriculostomía endoscópica premamilar (VEP) en la hidrocefalia: 24; Toma de biopsias
(TB): 5; evacuación de quistes tumorales (EQ): 3; endoscopías diagnósticas (ED): 5 y
colocación de catéter de derivación (V-P) bajo visualización endoscópica: 1. (Gráfico 1)
Las ventriculostomías del espacio premamilar
pudieron ser realizadas con cualquiera de los endoscopios utilizados, tanto rígidos como
flexibles. Los artroscopios rígidos nos permitieron penetrar al cuerno frontal del
ventrículo lateral, agujero de Monro (Figuras 5 y
10), parte anterior del 3er ventrículo (Figuras 6, 7, 8, 9 y 11), cisterna interpeduncular y cisterna prepóntica (Figuras
12, 13, 14 y 15). En el
caso de los broncoscopios, por ser flexibles y tener más rango de movimiento, fue posible
visualizar otras zonas no visibles con los rígidos. Además de los sitios descritos fue
permitido penetrar hasta la parte posterior del 3er ventrículo (Figuras 16, 17 y 18), el ángulo pontocerebeloso, región cuadrigeminal,
carrefour, cuerno occipital, cuerno esfenoidal; así como maniobrar fácilmente dentro de
cavidades quísticas. Las fenestraciones con los broncoscopios permitieron perforar
inicialmente el espacio premamilar con instrumentos finos de 1 ó 2 mm (Figura 7), a través del canal de trabajo y fueron
agrandadas posteriormente con el mismo fibroscopio. Las fenestraciones con los
artroscopios rígidos se realizaron directamente con la punta del equipo y posteriormente
penetramos hasta las cisternas interpeduncular y prepóntica (12, 13, 14, 15, 16, 17).
Las biopsias fueron tomadas exclusivamente con el
broncoscopio por tener un canal de trabajo que permite introducir una pinza para ello (Figura 3). Se tomaron 3 biopsias en quistes
tumorales del parénquima cerebral, 1 en un tumor de la parte posterior del 3er
ventrículo, y otra a nivel del vermis cerebeloso (a través del receso suprapineal). De
las 3 muestras examinadas en los portadores de quistes intraparenquimatosos, 2 de ellas
fueron positivas de astrocitomas Grado III (pacientes # 2 y 3). La muestra del 3er
paciente arrojó "Gliosis" y no se pudo determinar la etiología del tumor. A
este último un tiempo después se le realizó exéresis de un Meningioma quístico fronto
parietal (caso # 24). La biopsia del tumor de la parte posterior del 3er ventrículo
resultó ser de un Disgerminoma que ha cedido bajo los efectos de la radioterapia
(paciente # 15). Este paciente tenía una hidrocefalia no comunicante debido a
obstrucción del acueducto de Silvio por el tumor y fue resuelta en el mismo acto
quirúrgico mediante fenestración endoscópica. En casos como este pueden ser útiles los
procederes neuroendoscópicos por la solución postoperatoria de la hidrocefalia y por la
posibilidad de la obtención de la biopsia por encima del receso suprapineal (18). La
biopsia de la lesión del vermis cerebeloso no fue útil para diagnóstico (paciente #
19). Los artroscopios que hemos utilizado no tienen canal de trabajo por lo que resulta
imposible tomar muestras para Anatomía Patológica, contrario a los neuroendoscopios
rígidos actuales que sí permiten realizar biopsia por tener canal de trabajo (19).
La evacuación de los quistes tumorales fue
realizada con equipos flexibles, pero pensamos que en determinados casos puede ser
realizado con la punta de los artroscopios rígidos que poseamos, aunque no tengan canal
de trabajo. A su vez nos permitió tomar biopsias de las paredes del quiste y nódulo
mural.
Las endoscopías diagnósticas incluyen aquellos
casos en los que se confirmó la presencia de tumor (dudosa en la imagenología), ya sea
por visualización directa del mismo (caso # 12), o porque pudo determinarse la etiología
tumoral al analizar la biopsia anatomopatológicamente (casos # 2, 3 y 15); y un paciente
(caso # 20) en el que pudo clasificarse la hidrocefalia como post-hemorrágica al
encontrar hemosiderina en cisterna.interpeduncular después de hacer la ventriculostomía
(paciente No. 20) (Tabla 1).
La asistencia a la colocación de catéter de
derivación (V-P) se realizó con el broncoscopio (paciente # 20). Nos ayudamos con la
pinza de biopsia a través del canal de trabajo para sostener la punta del catéter
delante de la zona de visión de la fibra óptica. Esto nos permitió llevar la punta del
catéter hasta el espacio premamilar, sitio de colocación ideal recomendado por algunos
autores (20, 21, 22, 23, 24). Al paciente al que se le realizó derivación (V-P) fue
porque no quedaba ninguna duda de que no iba a resolver con la fenestración premamilar
por presentar hidrocefalia comunicante. Además, se le realizó ventriculostomía
premamilar previamente (en el mismo acto quirúrgico) encontrando restos de hemosiderina a
nivel de las arterias basilar, cerebrales posteriores y cerebelosas superiores como
consecuencia de una hemorragia subaracnoidea reciente. Una de las aplicaciones de la
neuroendoscopía es la correcta colocación del catéter intraventricular, cosa que no
siempre se logra cuando se hace "a ciegas" (14, 23, 25).
Las complicaciones directas debido a la
manipulación endoscópica fueron (Tabla. 1):
En caso de ventriculostomía del piso del 3er
ventrículo:
-Sangramiento
intraventricular.....................2 pacientes.
-Meningoencefalitis.......................................1
paciente.
-Arritmia
transitoria........................................2 pacientes.
-Diplopia
transitoria.......................................2 pacientes .
Sangrado
intraventricular: Uno de los casos presentaba un tumor en hígado con
metástasis en pulmón y cerebelo (paciente # 7). La lesión cerebelosa le provocó
hidrocefalia. A pesar de su poca perspectiva de vida se discutió el caso con los médicos
de cabecera y con los familiares determinándose utilizar el proceder como medida
"heroica". Este paciente, a pesar de tener un coagulograma dentro de límites
normales, tuvo un sangrado transquirúrgico importante y, aunque finalmente fue
controlado, falleció 24 horas después. Otro paciente (# 6) tuvo un sangrado
intraventricular que se controló rápidamente. Este mismo paciente se recuperó bien
después de la anestesia, pero horas después hizo un episodio de depresión de conciencia
sin mediar movimientos convulsivos. Se le realizó Tomografía Axial Computadorizada (TAC)
de urgencia que estaba dentro de límites normales. Mejoró rápidamente sin necesidad de
tratamiento médico. Días después comenzó con rigidez de nuca, cefalea y vómitos, y se
le confirmó una meningoencefalitis que evolucionó bien con antibióticoterapia (ver Tabla 1). El sangrado intraventricular
transoperatorio es una de las complicaciones más temidas por el peligro de no lograr
cerrar el vaso lesionado, aunque generalmente cesa después de un rato de irrigación con
Solución Salina (19, 26).
Arritmia transitoria:
Los pacientes 6 y 19 de la Tabla 1 presentaron
arritmia durante el acto quirúrgico. Ocurrió en el 1er caso durante el sangrado
transquirúrgico y cedió rápidamente. El otro paciente tuvo la arritmia cuando con el
broncoscopio tomábamos la biopsia del vermis cerebeloso a través del receso suprapineal
(que estaba abierto espontáneamente). Esto nos obligó a tomar una sola muestra que
finalmente no fue útil para diagnóstico.
Diplopia transitoria:
Ocurrió en los pacientes 1 y 17. Fue por toma del VI par y duró 2 días en cada uno,
desapareciendo de forma espontánea. Consideramos que esto fue debido a la hipertensión
intracraneal que se provoca durante la administración de solución salina
intraventricular en el transoperatorio.
Sobre la solución de la hidrocefalia en la
ventriculostomía (Gráfico 2): Hubo 5
pacientes que no resolvieron la hidrocefalia. Por tanto se consideró que tenían una
hidrocefalia comunicante que requería como única solución definitiva catéter de
derivación. A uno de ellos se le realizó VEP, y al comprobarse la etiología
post-hemorrágica de la hidrocefalia por restos de hemosiderina en la cisterna
interpeduncular, decidimos realizar derivación (V-P) bajo visualización endoscópica
(caso # 20). Su evolución post-operatoria fue satisfactoria. Otro paciente (caso # 11),
después de varios años con derivación ventrículo-peritoneal por estenosis acueductal,
comenzó con disfunción valvular que no resolvió con la colocación de catéteres, al
parecer por insuficiencia del peritoneo para la absorción del LCR. Durante todas estas
manipulaciones quirúrgicas había presentado meningoencefalitis. Fue necesario entonces
realizar VEP en dos ocasiones. Después de la 1era mejoró sustancialmente la
hidrocefalia, pero 3 semanas más tarde reapareció la misma. Se le repitió la
endoscopía y se observó que se mantenía abierto el espacio premamilar, aunque no
funcionaba. Requirió posteriormente varias intervenciones para colocación de catéteres
de derivación y presentó múltiples cuadros de sepsis de la herida abdominal y
consecuentes meningoencefalitis que dieron al traste con la vida del paciente. En otra
paciente se fenestró el espacio premamilar y se tomó muestra de posible lesión de
vermis cerebeloso, que no arrojó resultados positivos. Finalmente, por evolución no
satisfactoria, le colocamos catéter de derivación V-P (caso # 19). El paciente No. 10
presentó una hidrocefalia postraumática. No obstante el 4to ventrículo se observaba
dentro de límites normales y decidimos realizar VEP que transcurrió sin complicaciones
transquirúrgicas. La hidrocefalia no mejoró y el estado clínico del paciente obligó a
realizar derivación al exterior y ulteriormente derivación V-P. Durante la recuperación
post-quirúrgica de la última intervención este paciente presentó intenso sangramiento
digestivo alto por úlcera gástrica y falleció por Shock hipovolémico. El paciente No.
26 se mantuvo con hidrocefalia con posterioridad al proceder endoscópico por lo que se le
realizó derivación al peritoneo (15, 19, 26).
Una de las complicaciones más frecuentes que se
reportan en los pacientes a los que se les realiza endoscopía es la fístula de LCR. Sin
embargo, nosotros no tuvimos ningún paciente con fístula. Consideramos que la principal
causa de esto es que utilizábamos trefina en vez de trépano para el agujero craneal por
donde introducir el endoscopio. El hecho de emplear la trefina de 2,5 cm nos permite
volver a colocar el hueso. Además, la duramadre que se expone permite que la apertura de
la misma se haga en forma semicircular, de sólo 5 mm, y posteriormente cerrarla. Pero
incluso en los primeros pacientes a los que no se les cerraba la duramadre, la colocación
del fragmento de hueso encima de poliuretano impidió esta complicación. Encima del hueso
pasamos hilos de sutura anudados en el periostio. Es decir, el hecho de volver a colocar
el hueso por el agujero de entrada del endoscopio al cráneo disminuye mucho la
posibilidad de la fístula, contrariamente a lo que sucede cuando es sólo un agujero de
trépano (19).
Otras complicaciones reportadas que nosotros no
tuvimos fueron hemiplejía, dilatación pupilar de larga evolución, hematoma subdural,
ataxia y somnolencia(12, 15).
Como reportan otros autores conocemos que parte de
las complicaciones que hemos tenido son debidas a la poca modesta experiencia de 28
pacientes y que con el tiempo la técnica empleada debe ser mejorada (27).
Las posibilidades técnicas que nos brindaron los
equipos fueron:
1-.Con cualquiera de ellos es posible hacer la
fenestración del piso del 3er ventrículo. La débil estructura del túber cinéreum en
el espacio premamilar es perforada fácilmente con cualquier endoscopio independientemente
de que sea rígido o flexible.
2-.El broncoscopio tiene un canal de trabajo que nos
permite tomar biopsias, introducir electrocoaguladores monopolares o bipolares, balones
para ampliar perforaciones, irrigar o depletar los ventrículos durante la cirugía,
especialmente en caso de sangramientos o salida de sustancias coloides. Todos sus
instrumentos son flexibles por lo que existe la posibilidad de manipular la punta del
broncoscopio con uno de ellos dentro.
3-.Nuestros artroscopios no tienen canal de trabajo,
pero sí de irrigación y succión. Esto permite de una forma más operativa tratar los
sangramientos en las cavidades naturales del encéfalo.que en el caso del broncoscopio.
4-.El diámetro externo y la forma de la punta de
los endoscopios ha sido adecuado para introducirlos a través del espacio premamilar. A la
hora de escoger el endoscopio a utilizar debe observarse cuidadosamente la punta del
mismo. Hay algunos artroscopios cuyo lente queda unos milímetros por dentro de su vaina.
Esto tiende a comportarse como un borde tubular con una cavidad en el medio que pudiera
lesionar las arterias de las cisternas. Por otra parte, al introducir el equipo puede
acumularse tejido cerebral en esta pequeña cavidad en la punta del artroscopio que
dificulte la visión. Consideramos que estos artroscopios no deben ser utilizados para
neuroendoscopía, a menos que se rebaje la longitud de la vaina; de forma que el lente
sobresalga ligeramente por fuera de ella. Los endoscopios rígidos con los que hemos
trabajado pueden tener la visión del lente a 0 ó 30 grados de angulación. Nos fue más
cómodo usar el de 0 grados por tener una visión directa a la zona que se perfora del
piso del 3er ventrículo, cosa que no ocurre cuando la punta del lente es a 30 grados.
FUNDAMENTACION
ECONOMICA
El costo de un set básico para
neuroendoscopía (incluyendo un endoscopio rígido y uno flexible con sus respectivos
instrumentales; cámara, fuente de luz de Xenón, monitor, equipo de video) oscila entre
40 000 $ y 80 000 $ USD, en dependencia de las firmas a las que se le soliciten. Nosotros
hemos hecho contacto con firmas que nos han brindado un precio más barato donde pudiera
obtenerse a un costo de 25 000 $ USD. En este último caso, sabiendo que en nuestro
hospital existen varios sets ("Torres") con cámara, fuentes de luz, monitor y
equipo de video, si compramos únicamente los endoscopios rígidos con su instrumental su
costo sería de 5 500 $ USD y el de los flexibles 7 500 $ USD. Sin embargo, nosotros no
hemos comprado neuroendoscopios porque utilizamos un broncoscopio comprado en 1983 al que
no se le daba uso. Endoscopios como este los hay en diferentes hospitales y son utilizados
por las especialidades de Anestesia , Pneumología y Otorrinolaringología. Los
artroscopios rígidos utilizados por nosotros han sido los propios de las especialidades
de Ortopedia o Reumatología de nuestros hospitales. Es decir, no ha sido necesario
invertir dinero para la compra de equipos de neuroendoscopía, porque nos hemos adaptado a
los recursos y condiciones propias, no sólo de nuestro hospital, sino también de otros
centros del país.
FACTIBILIDAD
DE LA GENERALIZACION EN TODO EL PAIS
Si partimos de que en todos los hospitales
provinciales de Cuba hay "torres" para la cirugía laparoscópica,
artroscópica, endoluminal, broncoscópica, etc; perfectamente pudieramos realizar
procederes neuroendoscópicos con los medios con que contamos (fácilmente transportables
por su poco peso y tamaño). Mejor aún ha sido la posibilidad que hemos encontrado en
algunos hospitales a los que ni siquiera tenemos que llevar nuestros endoscopios por
utilizar los propios de ellos.
En nuestro país existen 22 servicios de
Neurocirugía. Sólo 2 no están incluidos en hospitales provinciales generales con
posibilidad de intervenciones laparoscópicas, artroscópicas, etc. Estos hospitales son
el CIREN y el INN. El CIREN tiene los equipos para neuroendoscopía. El INN no tiene
fuentes de luz, cámara de video, ni monitor; para acoplar el broncoscopio que nos
prestaron y con el que hacemos neuroendoscopía. No obstante la cercanía que existe entre
el INN y nuestro hospital (500 m) ha permitido fácilmente realizar las intervenciones
neuroendoscópicas a los pacientes del Instituto.
De todo lo anteriormente expuesto concluimos lo
siguiente: Debido al desarrollo de la cirugía endoscópica en Cuba en todos los servicios
de Neurocirugía (con excepción del INN) pudiera hacerse neuroendoscopía con soluciones
alternativas, es decir, utilizando los equipos de otras especialidades. Si cada uno de los
20 servicios de neurocirugía que tienen posibilidades de hacer la endoscopía con
soluciones alternativas, se fueran por la opción de comprar neuroendoscopios el MINSAP
tendría que hacer los siguientes gastos:
-Para cada servicio un endoscopio rígido y uno
flexible con instrumental: 12 500 $ USD.
-Los 20 servicios del país: 250 000 $.
Todos estos cálculos sin incluir otros equipos
(cámaras, fuentes de luz, monitor, videos). En caso de que tuvieran que adquirirlos
también se necesitaría invertir 25 000 $ USD por servicio y 500 000 $ USD en todo el
país.
CONCLUSIONES
1-.La neuroendoscopía puede ser realizada en
todos los hospitales con servicios de neurocirugía del país que cuenten con salones de
cirugía laparoscópica, artroscópica, endoluminal, etc; especialmente para la solución
de la hidrocefalia, entidad tan frecuente en nuestro quehacer cotidiano.
3-.Tanto con los broncoscopios flexibles como con
los artroscopios rígidos utilizados puede hacerse perfectamente la fenestración
premamilar en la hidrocefalia. Los artroscopios pueden ser utilizados para la
fenestración endoscópica del piso del 3er ventrículo, pero hay que hacerlo directamente
con la punta del equipo.
4-.Se garantiza una eficaz ubicación del extremo
ventricular del catéter de derivación ventrículo-peritoneal bajo visualización con el
broncoscopio.
5-.La maniobrabilidad del broncoscopio flexible
permite tomar muestras para biopsias de cualquier parte de los ventrículos o dentro de
los tumores quísticos.
6-.Los broncoscopios que tienen un canal de trabajo
sin sitio para irrigación ni succión, requieren de cierto entrenamiento que permita
realizar todas las funciones de forma alternante.
8-.Los artroscopios, que tienen canal para
irrigación y succión, permiten una constante circulación de líquido, acción
importante para la neuroendoscopía.
9-.La ventriculostomía es realmente útil en
pacientes con hidrocefalia triventricular, no así en los casos con hidrocefalia
comunicante.
10-.La craneotomía con trefina puede ser una
solución para evitar las fístulas de LCR, complicación tan frecuente en los procederes
neuroendoscópicos.
BIBLIOGRAFIA
1-.Davis L. Neurosurgical Surgery. Philadelphia: Lea
& Febiger, 1939:405.
2-.Dandy W.E. Cerebral Ventriculoscopy. Jhon Hopkins
Hosp Bull 33:189, 1922.
3-.Fay T., Grant F.C. Ventriculoscopy and
intraventricular photography in internal hydrocephalus. JAMA. 80:461-463, 1923.
4-.Mixter W.J. Ventriculoscopy and puncture of the
floor of the third ventricle. Boston Med Surg J 188:277-278, 1923.
5-.Putnam T.J. Treatment of hydrocephalus by
endoscopic coagulation of the choroid plexus. N Engl J Med 210:1373-1376, 1934.
6-.Putnam T.J. The surgical treatment of infantile
hydrocefalus. Surg Gynecol Obstet 76:171-182, 1943.
7-.Burman M.D. Myeloscopy or the directed
visualization of the spinal canal and its contents. L Bone Joint Surg 13:695, 1931.
8-.Stern EL. The spinascope: A new instrument for
visualizing the spinal canal and its contents. Med Rec 143:31, 1936.
9-.Pool JL. Direct visualization of dorsal nerve
roots of the cauda equina by means of a myeloscope. Arch Neurol Psychiatry 39:1308-1313,
1938.
10-.Pool JL. Myeloscopy: Intraspinal endoscopy. Surg
Clin North Am 37:1401-1402, 1957.
11-.Ferrer E. Comunicación personal. Agosto, 1995.
12-.Bognar L, Fekete Z, Konya E, Lekka N, Czirjak S:
[A new technic in the management of hydrocephalus: neuro-endoscopy]. Orv Hetil 1998 Sep
6;139(36):2129-34
13-. Gangemi M, Maiuri F, Donati P, Sigona L,
Iaconetta G, De Divitiis E: Neuroendoscopy. Personal experience, indications and limits. J
Neurosurg Sci 1998 Mar;42(1):1-10
14-.Kazunari O, Masamichi T: Instrumentation.
Techniques in Neurosurg. 1996. Vol 1, No. 3, 151-158
15-.Jones RFC, Stening WA, Brydon M: Endoscopic
third ventriculostomy. Neurosurgery. 26:86-92, 1990.
16-.Jones RFC, Kwok BCT, Stening WA, Vonau M:
Neuroendoscopic third ventriculostomy. A practical alternative to extracranial shunts in
non-communicating hydrocephalus. Acta Neurochir 1994 [Suppl] 61: 79-83.
17-.Jones RFC, Brazier DH, Kwok BCT, Stening WA,
Vonau M: Neuroendoscopic third ventriculostomy. Concepts in Neurosurgery, Vol. 7, 1995
18-.Robinson S, Cohen AR. The role of neuroendoscopy
in the treatment of pineal region tumors. Surg. Neurol, 48(4)360-365, Sep, 1997.
19-. De Divitiis O: Provision of a neuroendoscopy
service. The Southampton experience. J Neurosurg Sci 1998 Sep;42(3):137-43
20-.Griffith HB. Technique of fontanelle and
presutural ventriculoscopy and endoscopic ventricular surgery in infants. Child's Brain
1:359-393, 1975.
21-.Griebel R, Khan M, Tan L. CFS shunt
complications: An analysis of contributory factors. CNS 1:77-80, 1985.
22-..Sekhar LN, Moossy J, Guthkelch AN.
Malfunctioning ventriculoperitoneal shunts. J. Neurosurg 56:411-416, 1982.
23-..Mc Callum J. Combined frameless stereotaxy and
neuroendoscopy in placemente of intracranial shunt catheters. Pediatr Neurosurg, 26(3):
127-129, Mar, 1997
24-.Griffith HB. Endoneurosurgery: Endoscopic
intracraneal surgery. In: Symon L, et al. eds. Advances and Technical Standards in
neurosurgery, New York: Springer-Verkagm 1986; 14:2-24.
25-.Yamamoto M, Oka K, Nagasaka S, Tomonaga M:
Ventriculoscope-Guided Ventriculoperitoneal shunt and shunt revision. Technical note. Acta
Neurochir (Wien) 1994. 129: 85-88.
26-.Valenzuela S, Trellez A: Pediatric
neuroendoscopy in Chile. Analysis of the first 100 cases. Childs Nerv Syst 1999
Sep;15(9):457-60 Mortalidad (2%), morbilidad (7%), complicaciones (Fistula, hemorragia y
ventriculitis) y solución de la hidrocefalia (90%).
27-. Teo C, Rahman S, Boop FA, Cherny B:
Complications of endoscopic neurosurgery. Childs Nerv Syst 1996 May;12(5):248-53;
discussion 253.
Tabla 1
| N° |
Sexo |
Edad |
Diagnóstico |
Proceder Endoscópico |
Complicaciones inherentes al proceder endoscópico |
Instrumento empleados |
| 1 |
M |
24 |
Hidrocefalia no
comunicante. Tumor talámico izqdo. |
VEP |
Diplopia transitoria |
Broncoscopio |
| 2 |
M |
37 |
Tumor quístico frontal izqdo. |
EQ/ED |
No |
Broncoscopio |
| 3 |
M |
49 |
Tumor quístico talámico
izqdo. Hidrocefalia no comunicante. |
VEP EQ/ED |
No |
Broncoscopio |
| 4 |
F |
19 |
Hidrocefalia no
comunicante. Estenosis acueductal.
Disfunción de DVP. |
VEP |
No |
Broncoscopio |
| 5 |
F |
29 |
Hidrocefalia no
comunicante. Estenosis acueductal. |
VEP |
No |
Broncoscopio |
| 6 |
M |
44 |
Hidrocefalia no comunicante. |
VEP |
Sangrado IV. Arritmia
Meningoencefalitis |
Broncoscopio |
| 7 |
M |
45 |
Hidrocefalia no
comunicante. Tumor de pulmón derecho.
Metástasis cerebelosa y peritoneal. |
VEP |
Sangrado IV. (Fallecido) |
Broncoscopio |
| 8 |
M |
38 |
Hidrocefalia no comunicante. |
VEP |
No |
Broncoscopio |
| 9 |
M |
59 |
Hidrocefalia no
comunicante. Estenosis acueductal. |
VEP |
No |
Broncoscopio |
| 10 |
M |
25 |
Hidrocefalia no
comunicante. HSA postraumática. |
VEP |
No |
Broncoscopio |
| 11 |
M |
56 |
Hidrocefalia no comunicante. |
VEP |
No |
Broncoscopio |
| 12 |
M |
36 |
Hidrocefalia no
comunicante ya derivada ( Torkildsen ). Quiste coloide del III
ventrículo. |
ED |
No |
Broncoscopio |
| 13 |
F |
32 |
Hidrocefalia no
comunicante. Sospecha de tumor subtalámico |
VEP |
No |
Broncoscopio |
| 14 |
M |
31 |
Hidrocefalia no
comunicante. Tumor de APC I operado. |
VEP |
No |
Broncoscopio |
| 15 |
M |
25 |
Tumor supraselar y pineal. |
VEP TB/ED |
No |
Broncoscopio |
| 16 |
F |
11 |
Hidrocefalia no
comunicante. Estenosis acueductal. |
VEP |
No |
Broncoscopio |
| 17 |
M |
22 |
Hidrocefalia no
comunicante. Sospecha de T talámico. |
VEP |
Diplopia transitoria |
Broncoscopio |
| 18 |
F |
54 |
Hidrocefalia no
comunicante. T. cerebeloso hemiferico izqdo. |
VEP |
No |
Broncoscopio |
| 19 |
F |
49 |
Hidrocefalia no
comunicante. T. del Velo medular suoerior. |
VEP TB |
Arritmia |
Broncoscopio |
| 20 |
F |
77 |
Hidrocefalia no
comunicante. HSA |
VEP CEC/ED |
No |
Broncoscopio |
| 21 |
M |
29 |
Hidrocefalia no comunicante. |
VEP |
No |
Broncoscopio |
| 22 |
F |
77 |
Hidrocefalia no
comunicante. Tumor de APC derecho. |
VEP |
No |
Artroscopio |
| 23 |
M |
31 |
Hidrocefalia no comunicante. |
VEP |
No |
Artroscopio |
| 24 |
M |
58 |
Tumor frontoparietal izqdo. |
TB |
No |
Broncoscopio |
| 25 |
M |
31 |
Hidrocefalia no comunicante. |
VEP |
No |
Artroscopio |
| 26 |
F |
28 |
Hidrocefalia no
comunicante. Sospecha de tumor pineal. |
VEP |
No |
Artroscopio |
| 27 |
F |
18 |
Hidrocefalia no
comunicante. Estenosis acueductal. |
VEP |
No |
Artroscopio |
| 28 |
M |
60 |
Hidrocefalia no
comunicante. Tumor pineal. |
VEP |
No |
Artroscopio |
LEYENDA:
- VEP- Ventriculostomía endoscópica premamilar.
- EQ - Evacuación del quiste.
- ED - Endoscopía diagnóstica.
- TB - Toma de biopsia.
- CEC-Colocación endoscópica del catéter ventricular.
Gráfico
1
Gráfico
2
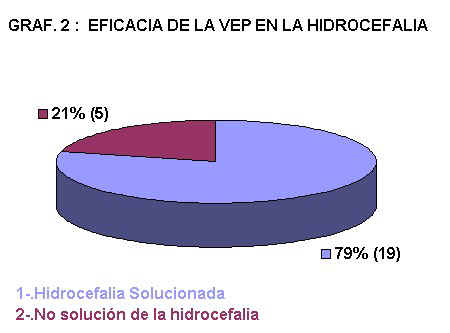
Figura 1
Durante la intervención
quirúrgica.
Figura
2a
Broncoscopio.

Figura 2b
Broncoscopio mostrando la movilidad de su
punta.
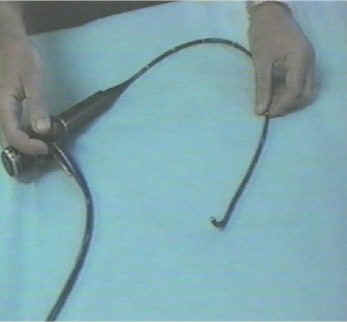
Figura 3
Punta del broncoscopio mostrando el ponche de
biopsia.
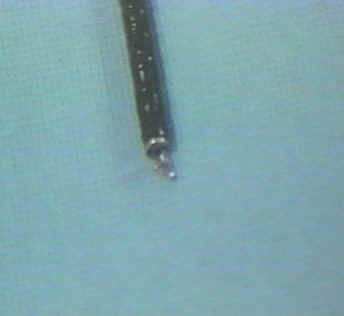
Figura 4
Parte de la Torre para acoplar la
cámara del broncoscopio.

Figura 5
Agujero de Monro con plexo coroides
(abajo y a la izquierda) y vena tálamo-estriada.
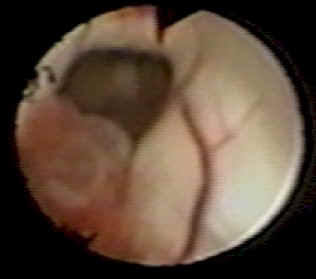
Figura
6
Espacio premamilar previo a la fenestración.
Obsérvese los cuerpos mamilares (abajo),
túber cinéreum (al centro) y el infundíbulo (arriba).
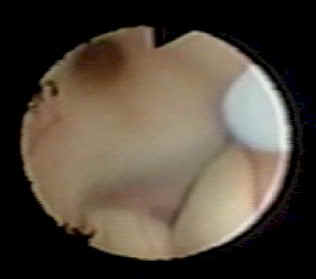
Figura 7
Espacio premamilar durante la
fenestración.
Apréciense los cuerpos mamilares
abajo y a la izquierda. El ponche de biopsia penetrando en el túber cinéreum.
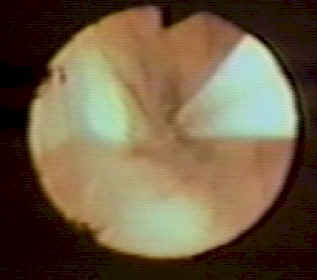
Figura 8
Espacio premamilar ya fenestrado.
A la izquierda cuerpos mamilares, al centro
la fenestración y a la derecha y arriba
una burbuja de aire
que dificulta visualizar el infundíbulo.
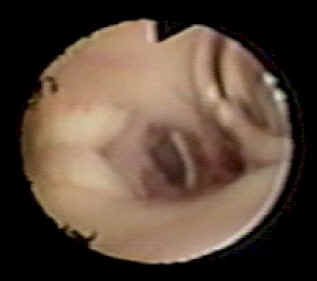
Figura
9
Imagen igual a la anterior, pero más
ampliada.
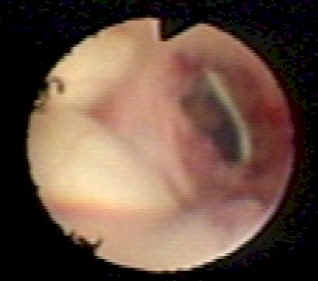
Figura10
Agujero de Monro con plexo coroides
arriba.
Se observa un catéter de
derivación en el piso del ventrículo lateral.
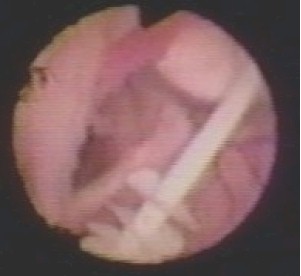
Figura
11
Piso del 3er Ventrículo fenestrado donde
observamos hemosiderina en paciente con hidrocefalia posthemorrágica.
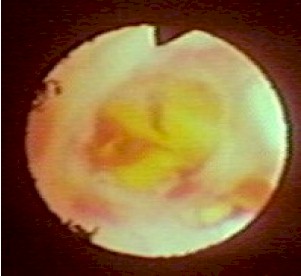
Figura
12
Cisterna prepontina con arteria basilar abajo
y a la izquierda.
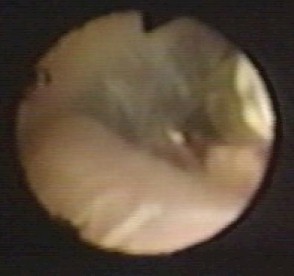
Figura 13
Arteria basilar donde ser
observa el nacimiento de una arteria cerebelosa.
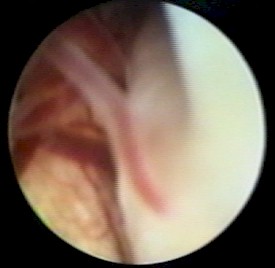
Figura
14
Arteria basilar y cerebelosa.
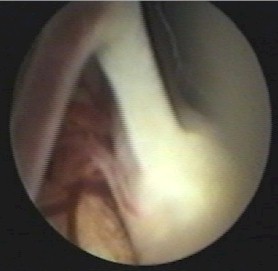
Figura
15
Cisterna prepontina con arteria basilar abajo
y clivus arriba y a la izquierda.
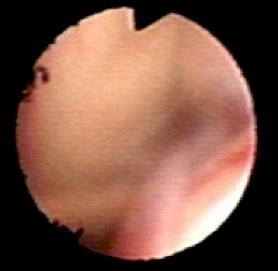
Figura 16
Parte posterior del 3er Ventrículo
con entrada del acueducto de Silvio (abajo),
comisura blanca posterior (al
centro) y receso suprapineal (arriba).
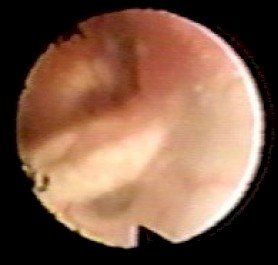
Figura 17
Parte posterior del 3er ventrículo
donde además se observa la tela coroidea y plexo coroides (arriba).
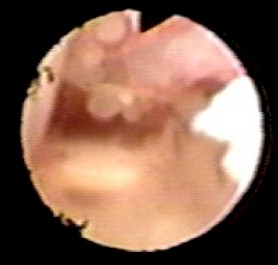
Figura 18
Parte posterior del 3er ventrículo
donde se observa un coágulo en la entrada del Acueducto de Silvio,
comisura blanca posterior, receso
suprapineal y comisura habenular.
|