|
|
Hipertensión Endocraneana
Autores:
Dr. Raúl Andrés Pérez Falero*; Dra. Angeles
de Lourdes Cardentey Pereda*;
*Especialista de 1er Grado en Neurocirugía. Institución: Hospital General "Abel Santamaría". SERVICIO DE
NEUROCIRUGIA. Resumen Introducción Desarrollo Tratamiento Bibliografía Enviar Comentarios Resumen Las características de cavidad semi-rígida confieren al cráneo y su contenido un comportamiento especial, con respecto a los demás órganos de la economía y se convierten los aumentos de presión en el interior en este espacio una amenaza contra la adecuada evolución de los pacientes con patologías intracraneales de etiologías disimiles. Efectuamos un estudio de la bibliografía publicada sobre el tema, además de nuestro criterio personal con respecto a los elementos que hemos podido evaluar en la practica clínica diaria. Se realiza una amplia revisión del tema exponiéndose los factores fisiopatológicos que intervienen en al mantenimiento de una homeostasis intracraneal, la influencia de las funciones vitales sobre dicha presión y otros aspectos de importancia. Las manifestaciones clínicas especificas de este síndrome son espuertas después de realizar un análisis de su fisiopatología. Se exponen los métodos para su medición así como la importancia de la utilización de estas evidencias en el establecimiento de un tratamiento adecuado, la terapéutica actualizada de esta entidad, así como los fundamentos de su aplicación Palabras claves: Presión intracraneal, hipertensión intracraneal, traumatismos craneoencefálicos, tumores intracraneales, hemorragia intracraneal, Monitorización intracraneal. El aumento de la presión intracraneana (PIC) es la causa mas frecuente de muerte en los pacientes neuroquirúrgicos y en gran parte de aquellos con enfermedades neurológicas. Los accidentes cerebrovasculares en sus formas isquémicas o hemorrágicas constituyen una de las primeras causas de muertes en los países desarrollados y también en el nuestro, además de los traumas craneoencefálico que son la principal causa de muerte en las personas entre 19 y 40 años; en ambos grupos ocurre un aumento de la presión dentro del recinto craneal, cuyo control es muy difícil dando al traste con la vida de muchos de estos enfermos. La terapia de estos pacientes con el desarrollo de las especialidades medicas ha dejado de ser un problema únicamente enfrentado por neurólogos y neurocirujanos y el neurointensivismo se independiza cada día mas como un método integral de manejo de las complicaciones intracraneales de accidentes vasculares encefálicos, tumores intracraneales, hidrocefalias y por ultimo el mas frecuente: los traumas craneoencefálico severos. A pesar de la asociación del edema cerebral con el aumento de la presión intracraneana, no fue hasta épocas recientes en que se ha obtenido información directa sobre la incidencia, magnitud y significación clínica de la hipertensión intracraneana, lo cual ha estado provocado en primer lugar por las dificultades para medir la PIC dentro de la cavidad craneal y en segundo lugar por los obstáculos encontrados al buscar un método fidedigno y seguro para el paciente. El primer reporte del monitoreo continuo de la PIC fue publicado en 1960 por Guillaume y Janney, mas tarde un ferviente investigador de la PIC, Lundberg, realizo el primer artículo sobre el monitoreo de una serie de pacientes (1,2). Durante los inicios de la década del 60 este autor y sus colegas analizaron el efecto de la hipertensión intracraneana experimental sobre el metabolismo cerebral y los signos vitales, trabajos que explicaron múltiples fenómenos hasta el momentos ignorados. Sin embargo no fue hasta una década mas tarde que se reportaron estudios de la PIC en grandes series. Fundamentos Anátomo-Fisiológicos. Concepto e Historia. Se define como PIC, aquella presión medida en el interior de la cavidad craneal y que es el resultado de la interacción entre el continente ( Cráneo ) y el contenido (Encéfalo, Liquido cefalorraquídeo y sangre) . El continente esta formado por un recipiente groseramente esférico constituido por una capa de hueso de variable grosor, además de poco o nada distensible en el adulto y que tiene dentro de sus características la de poseer varios agujeros de diferentes dimensiones. En su interior tiene tabiques formados por repliegues de la duramadre encefálica que influyen significativamente en los resultados de la respuesta de acomodación del tejido nervioso ante el aumento de presión, pero ¿Como sucede esto?, lo explicaremos mediante un ejemplo sencillo: Existen en el espacio intracraneal dos compartimentos: el supratentorial, ocupado por el cerebro y el infratentorial, en el cual se ubica el cerebelo y el tallo encefálico. Ambos compartimentos están separados por la tienda del cerebelo que se inserta en las clinoides posteriores a través de una circunferencia mayor y en las clinoides anteriores por la circunferencia menor; esta última determina un espacio que rodea al segmento mesencefálico del tallo cerebral y que puede ser mas o menos angosto, cuyas dimensiones varían entre 26 y 35 mms (Promedio-29,6 mms) (3). Cuando existe un aumento de la presión dentro del cráneo se hernian a través de este orificio los giros hipocampales de los lóbulos temporales y si el espacio es muy estrecho la superficie ventral del sistema nervioso sufre al ser comprimida y desplazada contra el clivus, provocando las hemorragias de Duret, es el llamado Síndrome de Herniación Central. De lo contrario cuando el espacio es suficiente como para permitir el paso del hipocampo se comprime entonces el tercer nervio y aparece de esta forma la dilatación pupilar, dando lugar al denominado Síndrome de Herniación Lateral; este ultimo signo no aparece en el síndrome de herniación central y puede dificultar el diagnostico sobre todo al personal medico que no esta familiarizado con la clínica neurológica. Las dimensiones de este agujero influyen de la misma forma en el síndrome por la hendidura de Kernohan, en el cual el pedúnculo contralateral al hipocampo herniado se comprime contra el borde libre tentorial del lado opuesto y provoca la aparición de defecto motor ipsilateral a la dilatación pupilar, categorizado como un falso signo de localización neurológica. El contenido de la cavidad craneana tiene tres componentes, el encéfalo, cuyo volumen ocupa el 80% del total y otros dos elementos que no por ser líquidos tienen menos importancia en los mecanismos tampones para el control del aumento en la PIC, ambos constituyen aproximadamente el 20%, dividido en iguales proporciones. Estos componentes son poco compresibles por lo cual el aumento en uno de ellos debe compensarse con la disminución proporcional de los restantes, dicha ley es conocida como la Doctrina de Monro-Kelly, la cual explica el comportamiento de los mecanismos Buffer o tampones en el control de la hipertensión endocraneana. Entre 1783 y 1823 Monro primeramente(4) y Kelly 40 años después plantearon dicha ley; pero aun no consideraban al líquido cefalorraquídeo (LCR) dentro de los elementos del contenido, mas tarde Burrows incorporó al LCR en 1846, después de las publicaciones de Magendie (5). Presión Intracraneal Normal.La presión en el estuche craneoraquídeo se midió por primera vez, mediante una aguja insertada en el espacio subaracnoideo lumbar y se determinó que en un paciente sentado, la columna de líquido ascendía hasta la unión cérvico-dorsal; aspecto que evidenciaba que la presión en este sistema no cumplía los principios de los vasos comunicantes de un sistema abierto y tampoco lo hacia como un sistema cerrado. Mas tarde Pollock y Boshes (6) determinaron que era el árbol vascular expuesto a la presión atmosférica el causante de esta peculiaridad en la PIC. La PIC no tiene un valor estable y se ve modificada por diversas situaciones fisiológicas que cambian el volumen de los elementos del contenido, por ejemplo: El pulso cardiaco provoca una verdadera inyección de sangre dentro de los vasos cerebrales, fenómeno que se traduce en una onda de 15mms de agua en la curva de monitoreo continuo de la PIC (7,8); de la misma forma el aumento de la presión en el sistema venoso como resultado de la inspiración respiratoria también modifica la PIC y se evidencia en el gráfico a través de ondas de mayor amplitud, si la añadimos al pulso cardiaco puede alcanzar hasta 45 mms de agua(7). Se han descrito otros factores como son la posición del individuo, las ondas de Traube-Hering-Meyer en la tensión arterial, maniobras de valsalva, el dolor, etc. Los valores normales establecidos para la PIC están entre 3-15 mms de Hg o 70-150 cms de agua, sin embargo algunos autores utilizan limites superiores para comenzar con el tratamiento en caso de hipertensión endocraneana por trauma craneoencefálico. Se considera que el trauma craneal grave es la única entidad donde se ha conseguido determinar evidente relación entre el nivel de la PIC y la gravedad del paciente, debido a que en este grupo de pacientes no se activan de forma adecuada los mecanismos tampones ante la hipertensión endocraneana y el cráneo se comporta como una cavidad totalmente cerrada. No sucede lo mismo en casos de tumores intracraneales, hidrocefalias de lenta progresión y otras causas, este fenómeno que parece estar explicado por el periodo en el cual se instala el aumento de la presión. Relación Volumen-Presión intracraneal.Al producirse hipercapnia de forma fisiológica casi se duplica el volumen de sangre en el lecho vascular, sin embargo esto no desencadena una elevación en la presión dentro del cráneo debido a que se produce un desplazamiento simultáneo de LCR(9). Cuando existen alteraciones previas en el contenido como: El edema cerebral, hematomas intracraneales, trastornos en la circulación del LCR, la vasodilatación causada por la hipercapnia es entonces poco tolerada y se eleva seguidamente la PIC(10); este ejemplo explica de manera breve la relación que existe entre el volumen intracraneal y la PIC, la cual expresamos con mayor objetividad en el gráfico de volumen-presión.
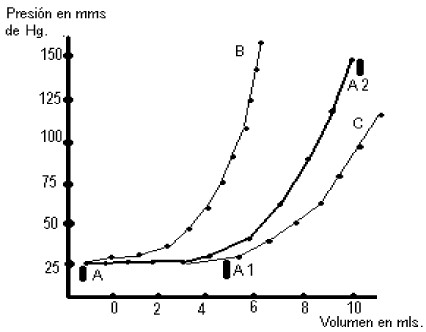 Figura 1: Gráfico de
relación volumen-presión.
Figura 1: Gráfico de
relación volumen-presión.
Fuente: Langfit, T.W., Weinstein, J.D.. Kasell. N.F., in Caveness, W.F. and Walker, A.D.,eds: Head Injury: Conference Procedings. Philadelphia, J.B. Lippincott Co., 1966
En dicho experimento el segmento horizontal de la curva (A-A1)fue denominado como periodo de compensación espacial pues ante aumentos progresivos de hasta 6 mls de liquido en el interior del cráneo, no hubo modificación en la PIC; sin embargo en el intervalo siguiente (A1-A2) si se produjo elevación en la presión por lo cual se le dio el nombre de periodo de descompensación espacial. Esta curva puede sufrir modificaciones en su curso, desplazándose hacia la izquierda (B) cuando exista un aumento en la resistencia (Elastance) del encéfalo, que puede obedecer a diferentes causas como: el edema anóxico ó isquémico, muy frecuente en el paciente politraumatizado. Otro de los motivos por los cuales puede suceder es que algún componente del contenido tenga dificultades para ser evacuado, por ejemplo, la hidrocefalia que se desarrolla en el caso de bloqueos subaracnoideos por sangre ó los infartos venosos por aumento de la presión en los senos intracraneales de etiología traumática o dificultades en general con el retorno venoso. La curva de volumen-presión puede inclinarse de la misma forma hacia la derecha, ( C ) modificación que evidencia un aumento de la tolerancia ante el aumento del volumen intracraneal, situación que con mas frecuencia se presenta en pacientes con atrofia cerebral de cualquier causa, estando incluidas como las más frecuentes aquellas secundarias a oclusión vascular, alcoholismo, ingestión de drogas, etc. Desde el punto de vista práctico este aumento en la adaptabilidad se verifica en pacientes en los cuales los estudios imagenológicos muestran colecciones intracraneales voluminosas y que clínicamente no tienen síntomas de aumento en la PIC o son muy vagos. En los párrafos anteriores hemos introducidos dos términos elementales en el estudio y evaluación de la PIC: Resistencia y Adaptabilidad. La resistencia (una traducción del inglés Elastance ) se interpreta como la capacidad que tiene el contenido, especialmente refiriéndonos al encéfalo, de ser comprimido ó de expandirse el propiamente dicho sin modificaciones substanciales en la PIC; estando alterada en situaciones como el edema cerebral húmedo, antiguamente denominados Vasogénico y Citotóxico o en el edema seco (Swelling Brain) por congestión vascular, que a propósito es mas frecuente en el niño o en el adulto mayor de 40 años, hipertenso y con tomografías interpretadas como normales y que algunos autores denominaron como Hipernormales. La adaptabilidad ( una traducción del inglés compliance ) se maneja como el espacio disponible dentro de la cavidad craneal para ser ocupado por determinado volumen; estando muy elevada en individuos de edad avanzada, alcohólicos, con atrofias cerebrales primarias. Se expresa como amplios cambios en el volumen sin variaciones importantes en la presión. La exposición de estos conceptos no tiene un objetivo meramente teórico, sino es el de aprender a ubicar a nuestro paciente en un punto de la curva volumen-presión y de esta forma conocer: 1ro- Cuales son sus posibilidades ante un aumento brusco ó progresivo del volumen intracraneal. 2do- Cuan efectivos han resultado los tratamientos aplicados. 3ro- Cuando es necesario realizar tratamiento quirúrgico. 4to- Que pronóstico de vida tiene y muchas otras que serian imposibles de responder sin conocer estos elementos. Existen algunos autores entre los cuales está Miller (11) que idearon métodos para conocer el efecto de los incrementos o disminuciones de volumen en un paciente con hipertensión endocraneana, por ejemplo: este autor injecta 1 ml de Solución Salina a través de una sonda intraventricular y miden el resultado que ellos denominaron respuesta volumen presión, este examen se ha utilizado incluso como uno de los parámetros a evaluar para retirar el tratamiento con Barbitúricos en el paciente con trauma craneal grave; otros prefieren hacer lo inverso para evitar las complicaciones sépticas como resultado de la inyección intraventricular, es decir retirar LCR y medir las variaciones de la PIC . Relación que existe entre la hipertensión endocraneana y los disturbios en las funciones del encéfalo. El encéfalo es capaz de responder de disímiles formas ante el aumento de la presión dentro de la cavidad; respuesta que depende de diversos factores que podríamos definir como el estado premórbido de dicho órgano. Abundantes son las muestras de como el aumento de la PIC en pacientes con Hidrocefalia, Pseudotumor cerebral y otras entidades no se correlaciona adecuadamente con la clínica del paciente, fenómeno que se ha justificado por el periodo de tiempo en el cual se instala el cuadro y la integridad de la autorregulación del lecho vascular cerebral y este último término se define como la capacidad del árbol vascular cerebral y específicamente de las arteriolas de controlar la presión sanguínea durante estados de variación en la tensión arterial media, incluso en grados extremos de esta última de la cual se establecieron 60 y 200 mms de Hg como valor inferior y superior respectivamente, específicamente para pacientes sanos. En otros artículos se han reportado cambios en la PIC con rangos entre 6 y 10 mms de Hg de presión intracraneal sin evidencias clínicas de hipoperfusión, gracias a la conservación de la autorregulación vascular. Situación muy diferente se ha encontrado en pacientes con traumas encefálicos en cualquiera de sus categorías; donde se maneja dos elementos inicialmente considerados como uno solo: Presión intracraneal regional(PICR) es aquella que se mide en el área adyacente al sitio de injuria, a decir hematomas, contusiones, edema, etc. y Presión intracraneal global(PICG) como aquella que se recoge en el interior de los ventrículos generalmente o en otro sitio común de medición como puede ser el espacio subaracnoideo o subdural y que a su vez es la que se considera como PIC, además de utilizarse para la toma de decisiones terapéuticas. Entre ambas presiones y la autorregulación de lecho vascular existe gran relación, pues a medida que sea mayor la PICR se necesitara de valores menores de PICG para afectar la respuesta vascular y mas dañinos serán lo efectos de su elevación.(12,13) Es decir que el aumento de la PIC se considera que afecta la función del encéfalo por dos mecanismos: 1ro- La interrupción de flujo sanguíneo por debajo del nivel crítico requerido para llevar al tejido nervioso una cantidad suficiente de O2 y nutrientes. 2do- La Herniación en determinadas regiones como la ocurrida a través del tentorio ó la hernia transforaminal que provoca compresión o isquemia directa del tallo encefálico; es decir que un hematoma localizado en el lóbulo temporal provoca una modificación suficiente la PICR como para comprimir el mescencéfalo sin modificar de forma evidente la PICG(12,13). Efectos de la hipertensión endocraneana sobre los signos vitales. Kocher fue el primero en asociar el aumento en la PIC a las variaciones en los signos vitales, sin embargo no fueron aceptados sus planteamientos hasta que los experimentos de Cushing demostraron similares resultados(14). La tensión arterial (TA) constituye el signo autonómico de mayor importancia durante el aumento de la presión intracraneana, pues esta se eleva para vencer la resistencia impuesta por la PIC a la entrada de la sangre. El momento en que sucede este fenómeno no está aun bien definido; pero se conoce que cuando la PIC se acerca o ha alcanzado el nivel de la presión arterial media (PAM) es necesario una mayor tensión arterial para garantizar la perfusión cerebral. La aparición de la respuesta o fenómeno de Cushing, como se conoce en la practica médica, constituye un signo ominoso para los pacientes con aumento postraumático de la PIC, sin embargo no indica pronóstico fatal como se pensó durante algún tiempo(15). Abundante es la experiencia en las salas de cuidados intensivos donde se realizan mediciones frecuentes de la PIC, y los clínicos se han percatado que una terapia adecuada aun en pacientes con la triada de Cushing puede modificar su evolución. Las variaciones en la frecuencia cardiaca ha recibido menos atención, independientemente de que ha sido demostrado como el signo autónomo de mayor importancia anta la expansión de un hematoma epidural(16). La respiración es el tercer parámetro vital que se evalúa en pacientes con elevación de la PIC. Muchos mecanismos autonómicos se ha planteado como la causa de estos, sobresaliendo aquellos que lo explican por inhibición de supresiones supramedulares. Durante el estadio diencefálico de la degradación rostrocaudal algunos pacientes tienen un patrón de respiración normal; pero la mayoría sufren de respiración periódica de Cheynes-Stokes. En estadios posteriores de la propia degradación como el nivel mesencefálico y protuberancial alto se modifica por hiperventilación neurogénica, y mas tarde durante el sufrimiento bulbar vuelve a ser normal para convertirse al final de este estadio en ataxia, apnea y paro respiratorio(17). Relación entre el flujo sanguíneo cerebral y la PIC.La circulación cerebral esta influenciada por las características anatómicas del lecho vascular y las correspondientes al cráneo(18), de modo que la tensión arterial tiene tres sitios fundamentales de resistencia: Las grandes arterias (39mm de Hg), los vasos piales (21 mm de Hg) y las venas (40 mm de Hg), similar a las arterias(19), aspectos que determinan las respuestas fisiológicas. La autorregulación se establece, según los criterios iniciales, por diferencia de presión a través de la pared vascular o presión transmural; por la tanto un aumento en la PIC o una disminución en la TA desencadenan una respuesta vasodilatadora ; de la misma forma que aparece vasoconstricción ante una caída en al PIC o elevación en la TA. Cuadro clínico de la hipertensión intracraneal.Mucho se ha escrito en este aspecto, sin embargo no existe un consenso en cuales son los síntomas y signos específicos del aumento de la presión en el interior del cráneo. Esta disquisición es provocada por lo variable que puede ser el comportamiento clínico de pacientes con aumento en la PIC y que depende de varios factores como pueden ser:
Se ha descrito una triada clásica que traduce elevación de la PIC, a decir cefalea, vómitos y papiledema; sin embargo algunos autores consideran solamente el papiledema, quienes plantean que por ejemplo: en el pseudotumor cerebral la cefalea no es el síntoma mas constante y los vómitos son infrecuentes y es bien sabido que en esta entidad los valores de la PIC pueden ser muy elevados. La cefalea se produce como consecuencia de la irritación de estructuras sensibles como los vasos, duramadre y nervios sensitivos, estructuras no siempre distorsionadas durante los episodios de hipertensión, Lundberg reportó episodios en sus pacientes de hasta 60 o 70 mms de Hg sin la presencia de cefalea u otros síntomas de hipertensión intracraneana(20-21). Los vómitos pueden tener múltiples causas, su control vegetativo por el SCN se encuentra en la porción mas caudal y dorsal del bulbo raquídeo, de modo que no esta explicado su mecanismo de producción en estas situaciones(21). El papiledema sin embargo esta directamente relacionado con un aumento de la presión en el espacio subaracnoideo y su continuación el espacio perióptico, este ultimo está anatómicamente esta formado por la extensión del espacio subaracnoideo intracraneal al rodear al nervio óptico después de su entrada en el canal óptico. En la actualidad el área del espacio subaracnoideo que rodea al nervio óptico constituye una de las regiones hacia donde se ha focalizado los estudios sobre el aumento de la PIC; por ejemplo se realizan estudios comparativos de los diámetros del nervio óptico a través del Ultrasonido Diagnostico y comparándolo con el contralateral y grupos controles(22). Otro de los medios utilizado ha sido la RMN, mediante la cual se mide el grado de protrusión del área papilar(Cabeza del Nervio Optico) y se ha demostrado su relación con la hipertensión endocraneana(23). No obstante es necesario descartar las causas oculares de papila de estasis, las que constituyen en la práctica motivo de error con frecuencia. Otros síntomas y signos relacionados con el aumento de la PIC son :
En este periodo existe modificación del volumen intracraneal, a expensas del desplazamiento de uno de los componentes líquidos, LCR y/o sangre. No se observan variaciones cuantitativas de la PIC y sí se produce de forma paulatina pueden no haber síntomas o signos sugestivos de tales disturbios. Segunda etapa.Durante esta etapa de subcompensación se produce una elevación de la PIC, generalmente ligera y comienzan a aparecer síntomas como consecuencia de la resistencia a la entrada de sangre al lecho vascular cerebral, dentro de los que se encuentran la hipertensión arterial y la bradicardia. Tercera etapa.Es el periodo en el cual los mecanismos buffer son insuficientes para compensar las variaciones en la magnitud de la PIC y comienza a desplazarse el tejido cerebral en dependencia de las líneas de fuerza, las herniaciones. La sintomatología es abundante y existen alteraciones como resultado de la Hipoxia-Isquemia cerebral. Los complementarios que pueden medir el funcionamiento encefálico muestran su bancarrota. Cuarta etapa.Coincide con los niveles bulbares de la degradación rostrocaudal, y traducen irreversibilidad del proceso. Las manifestaciones clínicas evidencia la agonía del control de las funciones autónomas. Es el periodo terminal. Métodos de medición de la PIC.Las primeras mediciones de presión en el LCR se realizaron en el espacio subaracnoideo lumbar por Quincke, quien planteó que los valores normales estaban entre 90-100 mms de agua(24). Años después Jackson midió la presión con este método en algunas condiciones patológicas y más tarde se utilizó en pacientes con traumas craneoencefálicos, estableciéndose criterios para la decisión de cirugía por encima de 200 mms de agua. Se plantearon numerosas objeciones a este método; pero las fundamentales eran:
Posteriormente se desarrollaron varios métodos y dispositivos con el mismo objetivo, como fueron las mediciones a nivel de:
Los sensores se han desarrollado de la misma forma que han evolucionado los sitios de su colocación , los iniciales estaban conectados a una columna de agua que era la encargada de trasmitir las variaciones de la presión, mas tarde fueron sistemas cerrados con balones sobre los cuales se ejercía la presión, todos con aditamentos que evitaban la contaminación de LCR y de este modo hacían al sistema fiable en cuanto a los resultados y protegidos contra la sepsis. En la actualidad existen algunos muy sofisticados como: aquellos acoplados a un sistema de fibra óptica que transmite la modificaciones en la posición de un pequeño espejo y su consiguiente lectura electrónica; pero por supuesto mientras mas sofisticados su manejo y cuidado exigen de personal mayormente entrenado. El sitio más utilizado para medir la PIC son los ventrículos laterales, específicamente su cuerno frontal no dominante, sobre los cuales Lundberg escribió una monografía en el monitoreo continuo de la PIC que recopiló toda la información previa sobre el tema y creo historia en la Neurocirugía. Este lugar ha permanecido como el sitio de elección para el estudio continuo de la PIC pues traduce con fiabilidad los aumentos de presión y permite además la evacuación de LCR durante los episodios hipertensivos. Beneficios del monitoreo continuo de la PIC. (27)
Desventajas del monitoreo continuo de la PIC.(27) Riesgos para el paciente:
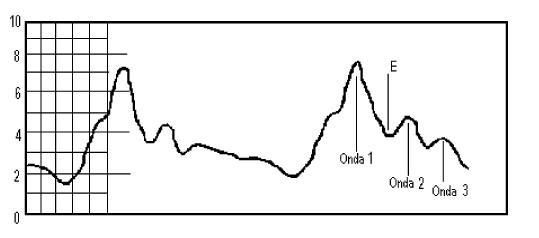
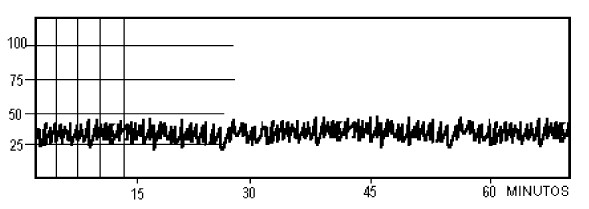
La presión intracraneal normal fluctúa entre los valores de 5 y 15 mms de Hg sobre la presión atmosférica. Su apariencia en los trazados de monitoreo de la PIC depende de factores relacionados con el método de medición, específicamente la velocidad con la cual se esta registrando y la influencia de las variaciones del contenido intravascular que se manifiestan por dos tipos de ondas, las correspondientes al latido cardiaco y las secundarias a las fases de la respiración pulmonar. El método mas utilizado para el monitoreo de la PIC es a través de la conexión del transductor a un equipo, que generalmente es capaz de proyectar en su pantalla de forma continua otros parámetros vitales además de las curvas de PIC. La velocidad con la cual se visualizan las curvas de la PIC determinan que tipo de gráfico se proyectara, por ejemplo: Cuando la velocidad del trazado es rápida, es decir se evalúa el comportamiento de las ondas en segundos, el gráfico muestra las ondas cardiacas de la PIC sobre las cuales mas tarde seremos explícitos y mientras mas lento sea el trazado se podrán ver las ondas respiratorias, por último cuando se estudien largos intervalos de tiempo se evaluará el comportamiento de la PIC según patrones descritos por Lundberg. Las ondas cardiacas u ondas de pulso del LCR se deben primariamente a la contracción del ventrículo izquierdo. Aparece una onda de pulso inicial correspondiente a la sístole cardiaca (Onda de percusión), seguida por una caída diastólica y una hendidura dicrota. Estas ondas del LCR semejan las del electrocardiograma. No obstante la forma y amplitud de estas ondas dependen de la entrada arterial, la salida venosa y el estado del resto de los componentes intracraneales(29).
Fuente: Lee, K. R., Hoff, J, T.: Intracraneal pressure. In Youmans, J. R.: Neurological Surgery, 4th Edition. W.B.Saunders Company., 1996
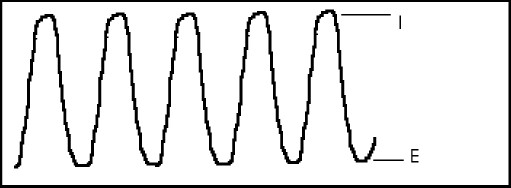
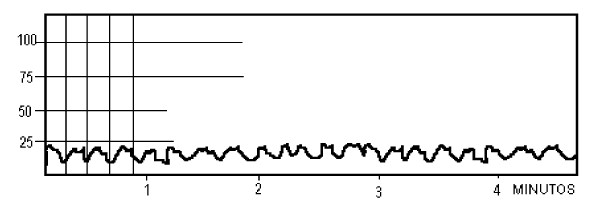
La fluctuación de la PIC con la respiración también esta influida por la velocidad de registro, no obstante su morfología es más constante y está determinada por las variaciones en la presión de las cavidades abdominales y torácica, que a su vez modifican el retorno venoso a la aurícula derecha(30).
Fuente: Lee, K. R., Hoff, J, T.: Intracraneal pressure. In Youmans, J. R.: Neurological Surgery, 4th Edition. W.B.Saunders Company., 1996
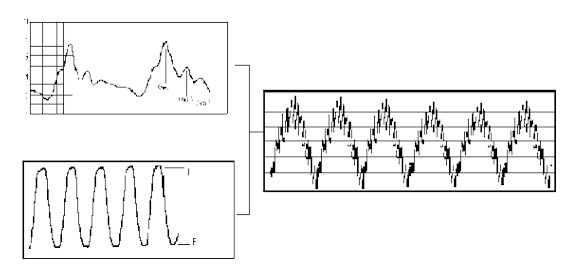
La superposición de ambas ondas en el mismo gráfico resultaría una imagen como la de la figura 4.
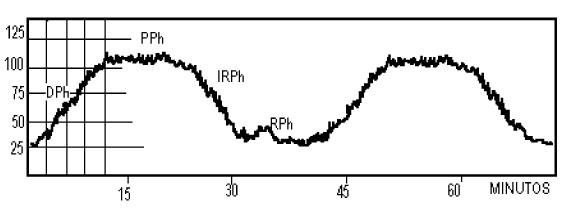
Fuente: Lee, K. R., Hoff, J, T.: Intracraneal pressure. In Youmans, J. R.: Neurological Surgery, 4th Edition. W.B.Saunders Company., 1996 Causas mas frecuentes de hipertensión intracraneal. Sin lugar a dudas, la causa mas común de aumento de la PIC son los traumas craneoencefálicos graves, de los cuales hasta el 54% de los pacientes son portadores de presiones por encima de 20 mmHg y el 92% de aquellos cuyas presiones son incontrolables, fallecen (31). Otra causa frecuente son las hemorragias intracraneales de diferentes etiologías, siendo los aneurismas rotos la mas común dentro de este grupo, y que provocan esta alteración por varios mecanismos: Efecto de masa inducido por la sangre extravasada, edema cerebral reactivo a la injuria del tejido nervioso, vasoespasmo e infartos cerebrales (32). Los tumores cerebrales, que se pueden manifestar de forma aguda, subaguda o crónica y que modifican la PIC por su propio efecto sobre los tejidos adyacentes o por bloqueo de la circulación de LCR. En las lesiones de crecimiento lento se puede ubicar al paciente en la porción ascendente de la curva volumen presión, con aumento substancial de la resistencia ( Elastance) y en la cual pequeños aumentos de volumen provocan significativos aumentos de los valores de la PIC. Oras causas no infrecuentes son: El pseudotumor cerebral, abscesos intracraneales, inflamaciones especificas o no, trombosis venosas y una muy discutida y que necesita estudios posteriores el edema seco o Swelling Brain, mas frecuente en niños con trauma craneal (33). Ondas de presión.El artículo de Lundberg en 1960 marcó pautas en el monitoreo de la PIC, pues se estudiaron 143 pacientes con síntomas y signos de hipertensión endocraneana (21). No obstante la mayor parte de los pacientes monitoreados por el autor eran portadores de tumores intracraneales, un grupo con hemorragias espontáneas y uno tercero con traumas craneoencefálicos. Se observaron tres tipos de ondas en función del tiempo y se denominaron como A, B y C. Ondas A ( Plateau Waves). Se observó en 21 de 48 pacientes a los cuales se les realizó la medición con catéter intraventricular. Todos tenían papiledema bilateral y tuvieron cefaleas intermitentes. Estas ondas aparecieron tanto durante el sueño como durante los estados de alerta, pudiéndose desencadenar por actividad mental o muscular en relación con el dolor, maniobras de enfermería, visitas de familiares, etc. La aparición de estas ondas fue también evidente desde el punto de vista clínico pues los pacientes despiertos comenzaron con cefalea, intranquilidad, toma del sensorio, confusión mental, movimientos sin objetivo y en aquellos pacientes inicialmente con algún grado de depresión del nivel de conciencia aparecieron fenómenos motores, trastornos del ritmo respiratorio, profundización de la inconsciencia. Estos síntomas eran abortados con la retirada de L.C.R. Es de señalar que algunos pacientes alcanzaron cifras de hasta 100 mms de Hg sin alteración alguna, consideramos esta relacionado con su patología de base porque la experiencia actual muestra que con valores muy inferiores se bloquea el flujo cerebral en pacientes traumatizados, elemento que tiene pronóstico ominoso. Lundberg hipotetizó en su artículo que dichas ondas eran secundarias a alteraciones del flujo, lo cual ha sido extensamente demostrado (34,35). Rosner y Becker consideran que las ondas A son expresión de un mecanismo compensatorio ante la disminución de la Presión de Perfusión Cerebral (P.P.C.) pues aparece durante la hipercapnia, cambios metabólicos y otras situaciones (36). La onda A tiene cuatro fases bien delimitadas (36), las cuales reflejan todo el mecanismo de autorregulación ante la disminución de la P.P.C.: Figura 5
Fuente: Lee, K. R., Hoff, J, T.: Intracraneal pressure. In Youmans, J. R.: Neurological Surgery, 4th Edition. W.B.Saunders Company., 1996 Ondas B.Son ondas menos específicas que las anteriores; pueden aparecer durante el sueño en individuos con valores normales de PIC, sin embargo son detectables en pacientes con clínica de hipertensión endocraneana, asociadas con frecuencia a respiración periódica del tipo Cheynes-Stokes (37).
Fuente: Lee, K. R., Hoff, J, T.: Intracraneal pressure. In Youmans, J. R.: Neurological Surgery, 4th Edition. W.B.Saunders Company., 1996
Su frecuencia es de una y media o dos por minuto y cuando están presentes en pacientes con aumento de la PIC por largos periodos traducen disfunción cerebral, Figura 6 Se piensa que su aparición esta relacionada con variaciones fisiológicas o patológicas del flujo sanguíneo cerebral, sin embargo los mecanismos específicos no están aun esclarecidos (38). Ondas C
Fuente: Lee, K. R., Hoff, J, T.: Intracraneal pressure. In Youmans, J. R.: Neurological Surgery, 4th Edition. W.B.Saunders Company., 1996 Estas ondas tienen mayor frecuencia pero menor amplitud que las descritas anteriormente. Ocurren en individuos normales por lo cual no tienen significación patológica. Son el resultado de la transmisión al espacio intracraneal de las ondas Traube-Hering-Mayer u ondas vasomotoras de la tensión arterial. Figura 7. Significación de las ondas de PIC.El monitoreo de la PIC tiene como objetivo predecir la elevación de las presión intracraneana por encima de los limites fisiológicos, una vez que los mecanismos tampones son insuficientes para su compensación. Es ideal que el diagnostico de la hipertensión endocraneana se realice antes de que existan manifestaciones clínicas, y mejor aún cuando está aun en niveles inferiores al límite superior de la normalidad, específicamente en el segmento "seguro" de la curva volumen-presión (C.V-P), donde cambios en el volumen intracraneal son bien tolerados pues la adaptabilidad (Compliance) es alta y la resistencia (Elastance) es escasa, mientras mas a la izquierda en la C.V-P se encuentre el paciente mayor es su capacidad compensadora. La primera manifestación de incapacidad para tolerar volúmenes intracraneales progresivos es la variación de la morfología en las ondas cardiacas y respiratorias, pues ambas traducen un aumento del componente sanguíneo intracraneal. Esta modificación en la tolerancia al volumen intracraneal puede obedecer a dos mecanismos fundamentales: Aumento de la resistencia ó vasodilatación cerebral; la determinación de la causa especifica se realiza analizando la razón entre ondas cardiacas y respiratorias; un valor bajo indica aumento de la resistencia (39). Varios maniobras se han diseñado para determinar la posición de un paciente en la C.V-P; Marmarou diseño el Indice volumen-presión (I.V-P), definido como la el volumen de líquido necesario para elevar la presión de apertura 10 veces (40). Esta medición describe la relación volumen-presión para un rango de valores de PIC. El calculo asume que el logaritmo matemático de la PIC tiene una relación lineal con el volumen añadido y una desviación correspondiente al valor del I.V-P., mientras menor es el I.V-P menos espacio disponible existe para acomodar nuevos volúmenes (41). Otros autores como Miller (11) y Wilkinson (42) diseñaron la Respuesta volumen-presión y la Reserva volumen-presión, respectivamente, mediante la inyección de determinados volúmenes de Solución Salina con el objetivo de evaluar la capacidad de los tampones. Estos procederes tienen como inconvenientes la posibilidad de sepsis, especialmente por Staphylacoccus epidermidis, la administración de volúmenes intracraneales que ocasionalmente provocaban hipertensiones mantenidas, además la limitación en el monitoreo continuo de los pacientes. Por estos motivos se desarrolló el sistema para el análisis de las ondas cardiacas, pues estas son la imagen de la entrada en el interior del árbol vascular cerebral de un volumen constante y relativamente estable, el gasto cardiaco cerebral, por lo tanto un cambio en la amplitud expresa un cambio en la relación volumen presión ó un cambio en la cantidad de sangre que penetra al cráneo. Este último parámetro es de difícil medición pues depende del gasto cardiaco, de la resistencia vascular cerebral en cada latido y del drenaje venoso. Por todas estas razones la relación entre la amplitud del pulso y la resistencia cerebral permanece poco definida. No obstante, la morfología de la onda cardiaca se relaciona con la PIC pues para valores normales de esta última la onda de percusión es la mas alta Figura 2, a diferencia de la hipertensión intracraneana donde la onda Tidal alcanza una amplitud superior. Tratamiento. El manejo de la hipertensión endocraneana se ha modificado de forma substancial desde la introducción de las modernas formas de neuromonitoreo, resultando inadmisible el empleo de drogas u otros medios sin la correspondiente justificación fisiopatológica en el caso especifico. Hemos hablado al inicio de la revisión de los componentes del contenido intracraneal, tejido encefálico, sangre y líquido cefalorraquídeo y de como cada uno de estos puede aumentar de forma independiente ó en algunas ocasiones mas de uno a la vez; este última variante es muy frecuente en los traumatismos craneoencefálicos. Los avances actuales permiten que el tratamiento de los aumentos en la PIC sea causa-dirigido. Ejemplo: Si existe una obstrucción en la circulación del LCR por un sellaje de las cisternas basales, como consecuencia de una hemorragia subaracnoidea ó una meningoencefalitis bacteriana, el tratamiento debe ir encaminado a diminuir la producción de LCR y/ó vencer la obstrucción, por varios métodos que no son el objetivo de este tema. Si existe un hematoma subdural crónico que este provocando un conflicto de espacio es indicativa su evacuación quirúrgica; pero sin duda que la causa mas frecuente de hipertensión endocraneana lo constituyen los traumatismos craneoencefálicos y los tumores cerebrales a los cuales dedicaremos un espacio mayor. Los traumas craneales pueden incrementar la PIC por disímiles mecanismos dentro de los cuales el edema cerebral, la congestión vascular cerebral y los hematomas cerebrales son los mas frecuentes; sin embargo una hidrocefalia secundaria a un hematoma de fosa posterior ó a una hemorragia subaracnoidea postraumática no son excepcionales. El manejo intensivo del trauma craneoencefálico a través del monitoreo de la PIC, la saturación de oxigeno en el bulbo de la vena yugular y la medición contínua de la presión arterial media nos indican con relativa seguridad cual es la causa especifica del aumento en la PIC. Ejemplo: Una vez que se ha descartado un hematoma intracraneal por una Tomografía Computada de urgencia y solo aparecen en la imagen lesiones difusas, a decir edema cerebral ó focos de hemorragia y contusión sin criterio quirúrgico, es elemental conocer el estado de la autorregulación cerebral para aplicar los diversos métodos disponibles para el tratamiento de la hipertensión endocraneana. La utilización de los diuréticos osmóticos ( Manitol 20%) en un paciente con daño extenso de la barrera hematoencefálica puede complicar su evolución, al igual que el uso indiscriminado de la hiperventilación ó los barbitúricos. En el caso de los tumores intracraneales, el edema cerebral en cualquiera de sus variantes ó la hidrocefalia provocan aumento de la PIC, por lo cual el uso de esteroides ó una derivación de la circulación del LCR deben tener su fundamento en la causa directa. El tratamiento lo dividiremos en medidas clínicas y quirúrgicas, haciendo énfasis en el primer grupo. Medidas Clínicas
Posición del Paciente. Por mucho tiempo fue criterio generalizado la elevación de la cabeza en los pacientes con traumas craneoencefálicos graves de 30 a 45 grados sobre el nivel de la aurícula izquierda; sin embargo estudios ulteriores no han demostrado variaciones significativas de la PIC con las modificaciones en la altura de la cabeza. Existen factores hipotéticos que justifican tales conductas, de estos el mas universal refiere que la elevación de la cabeza mejora el drenaje venoso intracraneal; criterio con el que no todos los autores están de acuerdo. Ejemplo: Algunos plantean que el componente vascular venoso intracraneal esta de hecho reducido durante la hipertensión endocraneana pues las venas superficiales se colapsan; pero ¿sucede lo mismo con los senos venosos, cuyas paredes son de origen dural y de hecho resistentes a la compresión?; por otra parte otros consideran que las modificaciones en la presión son provocadas por cambios hidrostáticos.(40) En contra de esta posición algunos autores fundamentan que el Fowler disminuye el retorno venoso y por lo tanto una caída del gasto cardiaco, con la consiguiente disminución de la presión de perfusión cerebral.(37) No obstante existen algunas afirmaciones con respecto a la posición corporal cuya veracidad se ha demostrado; nos referimos a las modificaciones provocadas en el retorno venoso por la lateralización del cuello con la correspondiente compresión de venas yugulares, la cual puede provocarse además por la gasa utilizada para fijar el tubo endotraqueal. En conclusión la posición de la cabeza debe valorarse en cada paciente de forma individual, es decir posición optimizada. Ir a Medidas ClínicasHiperventilación Mecánica. El primer aspecto que debemos mencionar no esta directamente relacionado con la ventilación mecánica y sí con la importancia de garantizar una vía aérea permeable y con suficiente O2 para la correcta difusión. En los pacientes con depresión del nivel de consciencia el estímulo autonómico a la respiración esta con frecuencia disminuido, además de la obstrucción en las vías aéreas, esta situación provoca aumento de la presión intratoracica e interferencia con el drenaje venoso yugular(43-44-45). El problema fundamental resultado de la hipoventilación es la hipercapnia, alteración que induce el metabolismo anaerobio con la consecuente acidosis láctica y daño de la membrana celular, además de fenómenos de robo vascular en las regiones del encéfalo con daño de la autorregulación, de hecho muy frecuente en el trauma craneal donde la respuesta del lecho vascular a las modificaciones de la presión de CO2 no es uniforme en tiempo ni espacio. La vasoplejía, por daño de la capacidad autorreguladora provoca desplazamiento de sangre desde el tejido lesionado hacia el sano como consecuencia de la vasodilatación de este ultimo ante la hipercapnia.(46-47) Desde el punto de vista teórico la hiperventilación debe provocar un resultado contrario, la hipocapnia, estado que debe desencadenar una vasoconstrición inducida por la alcalosis del medio interno y como resultado disminución del componente intravascular; sin embargo todo no sucede de esta manera. En los pacientes con traumas craneoencefálicos existen conflictos que provocan disyuntivas terapéuticas, por ejemplo: la respuesta a la hipocapnia está reducida y además cuando aparece tiene una duración efímera. Tal situación dificulta la aplicación del método hiperventilatorio. Si analizamos situaciones análogas desde el punto de vista bioquímico veremos que la reacción entre el ácido láctico y el bicarbonato consume este ultimo compuesto, buffer elemental en el mantenimiento del equilibrio ácido-básico, y aun después de expulsado el CO2 resultante de la reacción descrita, prevalece la acidosis del medio celular que provoca vasodilatación e hipertensión endocraneana. La suspención de la hiperventilación en tal situación motiva aumento de la PIC por fenómeno de rebote. En el tratamiento de los pacientes con lesiones postraumáticas severas del S.N.C. se preconizo inicialmente la restricción de fluidos; sin embargo en la actualidad esta demostrado la utilidad de las soluciones expansoras del plasma e incluso catecolaminas, siempre que se utilicen simultáneamente con medidas para disminuir la PIC, como: El drenaje de LCR a través de catéter intraventricular, el uso de diuréticos osmóticos y otros métodos. El objetivo primordial de todo el tratamiento antihipertensivo endocraneal, a decir las medidas encaminadas a reducir la PIC e incrementar la presión arterial media, es mantener una presión de perfusión cerebral adecuada a expensas de cualquier otro parámetro. En estudios recientes se ha evidenciado la ausencia de correlación entre la cantidad de Sodio y fluidos administrados durante las primeras 72 horas con la PIC y el estado al egreso de los pacientes.(48) La mortalidad de los pacientes con traumas craneales se duplica en presencia de hipotensión arterial, por lo tanto el manejo de fluidos debe ser optimizado para cada caso. Otra de las vertientes para las cuales se administran los líquidos en infusión son las llamadas dosis de resucitación, que se aplican durante los estados de hipotensión arterial en pacientes con traumas craneales asociados ó no. Dentro de sus efectos se plantean:
Los compuestos mas utilizados son el Ringer-Lactato a dosis de 40 ml / Kg. , la Solución Salina Hipertónica 7.5% a dosis de 4 ml / kg. y el Dextran.(49) Diuréticos Osmóticos. Se han utilizado varios diuréticos con propiedades osmóticas en la tratamiento de la hipertensión endocraneana, dentro de estos el Manitol es preferido pues disminuye la PIC por varios mecanismos, además que modifica de forma substancial la homeostasis intracraneal.(50-51) Efectos ventajosos del Manitol:
Estas propiedades son mas significativas cuando la autorregulación esta intacta, de lo contrario si existe un extenso daño la barrera hematoencefálica disminuyen sus ventajas y en tal situación la extravasación del diurético puede provocar el efecto osmótico inverso y por lo tanto aumento en la PIC. Efectos adversos del Manitol.
La dosis recomendada de Manitol % es de 0.25 - 2 g / Kg. / Dosis cada 4 u 8 horas, independientemente que se ha utilizado en infusión continua ó en dosis hiperfraccionadas (Cada 2 horas). El pico de acción esta entre 15 a 20 minutos después de la infusión. La utilización simultánea de diuréticos de Asa, específicamente la Furosemida (Lasix), incrementa el efecto del Manitol. Su administración debe hacerse 15 minutos después del osmótico. Por todos los efectos adversos del Manitol se han estado utilizando otros compuestos en el tratamiento del trauma craneal, sobre todo para sustituir sus efectos sobre el volumen intravascular, la presión intracraneal y la capacidad de modificar las características reológicas, nos referimos a la Solución Salina Hipertónica al 3%, 5% ó 7.5% con los cuales los resultados son buenos pero aun el numero de pacientes es muy limitado.(52) El uso de los esteroides en el tratamiento de la hipertensión endocraneana ha sido ampliamente estudiado, independientemente que existen aun divergencias en el análisis de los resultados (53-54) Esta demostrado la ausencia de efectos beneficiosos en el edema postraumático ó en el producido en los accidentes vasculares encefálicos, infartos ó edema perihemorrágico. Sin embargo el edema presente en los tumores intracraneales es altamente reversible con el uso de Dexametazona y Alfametilprednisolona; aunque el efecto es de corta duración, por ejemplo: se plantea que el pico de respuesta a los esteroides en los tumores intracraneales metastásicos alcanza una semana, periodo después del cual declina su efecto. Los mecanismos a través de los cuales actúan no están dilucidados, no obstante se plantean hipótesis como la estabilización de las membranas lisosómicas y la barrera hematoencefálica , además de la disminución de la respuesta del sistema inmune ante la presencia de un tejido con características anormales al resto del tejido circundante. Se han ensayado otros esteroides como el Tirilazad, medicamento que se empleo inicialmente en el tratamiento del trauma espinal grave con compromiso neurológico y mas tarde se extendió su uso a los tumores cerebrales. Las dosis ideales aun no están determinadas y se usan regímenes a bajas dosis de Dexametazona, 10 mgs de dosis de carga seguidos por 4 mgs por vía endovenosa cada 6 horas. La primitiva observación de Horsley, en 1937, acerca de que el Pentobarbital producía un descenso en la presión del liquido cefalorraquídeo no fue aprovechada hasta 36 años después por Shapiro y col.(55) Este grupo de drogas se utilizan en el tratamiento de la hipertensión intracraneal cuando las demás medidas han fracasado. Efectos ventajosos de los Barbitúricos.
Efectos adversos de los Barbitúricos.
Un punto interesante lo constituye el tipo de barbitúrico a emplear, pues si se desea un efecto rápido debe utilizarse el Thiopental (57) pero el de mas frecuente uso en la practica es el Pentobarbital a dosis de carga de 3 - 10 mgs / kg. administrados en un periodo entre media hora y 3 horas, la dosis de mantenimiento será de 0.5 - 3 mg / kg. / hora (58). Algunos autores consideran elemental el seguimiento de la barbituremia a diferencias de otros que no la consideran necesaria pues las dosis aplicadas deben ser personalizadas, por lo cual sus valores en sangre no traducen su efecto, ni toxicidad. ¿Cuando debe retirarse la terapia con barbitúricos?. Varias e imprecisas respuestas pueden darse; sin embargo existen criterios para suspender la terapia como:
El uso de la hipotermia convencional, denominándose así al descenso de la temperatura corporal por debajo de 30° centígrados, se utilizó en el tratamiento de la hipertensión intracraneal puesto que disminuye la actividad metabólica, el consumo de oxigeno y el flujo sanguíneo cerebral. No obstante el gran numero de complicaciones que se producían, además de las dificultades técnicas para mantener esta temperatura limitaron su aplicación practica. Se han realizado estudios con hipotermia moderada que ha arrojado efectos beneficiosos sobre los aumentos de PIC, pero el escaso numero de pacientes exige el análisis de grupos mayores. (59) Recientemente se ha utilizado la Indometacina en el tratamiento de la hipertensión endocraneal, sugiriéndose que el mecanismo de acción es el siguiente: Disminución del flujo sanguíneo cerebral asociado a incremento en la diferencia arteriovenosa de O2, sin afectar la captación cerebral de O2, modificar la diferencia arteriovenosa de Lactato ni el índice Oxigeno-Lactato.(60) En estudios realizados en niños con lesiones cerebrales e incrementos agudos en la PIC se ha concluido que puede incrementar la perfusión cerebral global e incremento de la saturación de O2 en el bulbo de la vena yugular.(61-62) La indometacina se ha administrado por varias vías incluida la rectal, la dosis de carga recomendada es de 0.4 mg / kg. seguida de una infusión de 0.4 mg / kg. / hora; el periodo de acción es de aproximadamente 6 horas sin evidencias de adaptación en este periodo.(63) Algunos autores la han utilizado asociada a la hiperventilación sin demostrarse un patrón de comportamiento con el uso combinado de estos métodos terapéuticos.(64) La aplicación del oxigeno hiperbárico tiene su fundamento en la disminución del flujo sanguíneo cerebral y el incremento de la oxigenación tisular. Su aplicación clínica ha demostrado mejoría en los índices de mortalidad de los grupos tratados con respecto al control, 42 % vs 17% respectivamente. Pero la ausencia de recuperación de aquellos pacientes en grupos de baja calidad de vida limita su uso, es decir que aumenta el numero de pacientes con secuelas graves.(65) Los métodos quirúrgicos para la solución de conflictos de presión intracraneal los dividiremos en dos grupos: Procederes para lesiones con efecto de masa y aquellos para el tratamiento en lesiones no evacuables. En el primer grupo se incluyen pacientes con hematomas intracraneales postraumáticos, tumores cerebrales, hidrocefalias, abscesos cerebrales, etc. en los cuales esta demostrado que la remoción quirúrgica de la lesión resuelve de forma total o parcial el aumento de la PIC con unos resultados indiscutibles, a este tipo de tratamiento lo denominamos específicos El manejo quirúrgico de pacientes sin lesiones removibles, que denominamos tratamiento inespecífico, es el mas controversial. Son individuos con lesiones difusas que aunque aumentan la PIC, no tienen volumen como para ser removidas de forma independiente del parénquima adyacente. Se aplican dos técnicas fundamentales: La descompresión ósea y/ó remoción de tejido cerebral. Cuando se realizan las descompresiones óseas los sitios de mas frecuente ataque son los huesos temporales, que se resecan y abre la duramadre subyacente; otra técnica quirúrgica son las descompresiones bifrontales sin apertura dural.(66) La resección de tejido cerebral es también un método útil, pero con este debemos ser mas cuidadosos pues debe resecarse tejido poco ó nada elocuente en las funciones encefálicas. Los sitios escogidos son generalmente los lóbulos temporales y frontales, preferentemente no dominantes; sin embargo solo el mapeo cortical transquirúrgico es capaz de asegurar que región cortical tiene una u otra función Ambos métodos han demostrado ser beneficiosos en el tratamiento de pacientes con traumas craneales, disminuyendo la morbi-mortalidad por esta causa. 1-Guillaume,J.,Janny,P. Manometrie Intracranienne continue. Interet Phisiopatologique et Clinique de la methode. Press. Med. 1951; 59:953-955 2-Lundberg,N. Continuous recording and control of ventricular fluid pressure in neurosurgical practice. Acta Psychiat. Scand. 1960; 36: suppl.149: 1-193 3- Ono, M., Ono, M., Rhoton, A. L. Jr, Barry,M. Microsurgical anatomy of the region of the tentorial inscisura. J.Neurosurg. 1984; 60: 365-399 4-Monro, A. Observation of the structure and function of the nervous system. Edinburg, Creech and Jhonson, 1783 5-Burrows, G. Disorders of the cerebral circulation. London, 1846 6-Pollock, l. J., Boshes, B.: Cerebrospinal fluid pressure. Arch. Neurol. Psychiat. 1936; 36:931-974 7-Bradley, K. C. Cerebrospinal fluid pressure . J. Neurol. Neurosurg. Psychiat.1970; 33:387-397 8- Dunbar, H. S., Guthrie, T. C., Karpell, B. A study of cerebrospinal fluid pulse wave. Arch. Neurol. 1966; 14: 624-639 9-White,J.C.,Verlot, M., Selverstone B. Beecher, H. K. Changes in brain volume during anesthesia. The effects of anoxia and hipercapnia. Arch. Surg. 1942; 44: 1-21 10-Hayashi, M., Kobayashi, H., Fuji, H.,Yamamoto, S. Ventricular size and isotope cisternography in patients with acute transient rises of intracraneal pressure (Plateau Waves). J. Neurosurg.1982; 57: 797-803 11-Miller, J. D., Gabiri, J. Intracranial volume-pressure relationships during continuous monitoring of ventricular fluids pressure. In Brock, M., Dietz, H.: Intracranial pressure experimental and clinical aspects. Berling. Springer-Verlag,1972 12-Weaver, D. D., Winn, H. R., Harrison ,K. M. Differential intracraneal pressure in patients with unilateral mass lesions. J. Neurosurg. 1982; 56:660-665 13-Wozney, P., Yonas, H., Latchaw, R. E., Gur, D., Good,. W. Central herniation revealed by focal decrease in regional blood flow without elevation of intracraneal pressure: A case report. Neurosurgery.1985; 17:641-644 14-Kocher, T.: Hirnerschutterung, Hirndruck und chirurgishe Eingriffe bei Hirnerkrankungen Nothnagl’s specialle pathologie und therapie. 1901; Biid ix,3 teil, 2 Abteilung, s 81 15-Cushing H. Some experimental and clinical observations concerning states of increased intracraneal tension. Am. J. Med. Sci. 1902; 124:375-400 16-Durward, Q. J., Amacher, A. L., Delmaestro, R., Sibbadl , W. J. The influence of the systemic arterial pressure on the development of cerebral vasogenic edema. J. Neurosurg. 1983; 59:805-809 17-Jackson, J.H.: Neurological Fragment. XV. Superior and subordinate centers of the lower level. Lancet. 1895; 1:476-478 18-Shapiro, H. M., Langfitt, T. W., Weinstein, J. D. Compression of the cerebral vessels by intracraneal hypertension. II. Morphological evidence for collapse of vessels. Acta Neurochir. 1966; 12:223-233 19-Stern, W. E. Good, R. G. Studies of the effects of hypothermia upon cerebrospinal fluid oxygen tension and carotid blood flow. Surgery. 1960; 48:13-30 20-Wolff, H.G. Headache and other head pain. New York. Oxford University Press, 1963 21-Lundberg, N. Continuos recording and control of ventricular fluid pressure in neurosurgical practice. Acta Psychiatry, Scand. 1960; 36:1-1993 22-Hansen, H. C., Helmke, K. The subaracnoid space surrounding the optic nerves. An ultrasound study of the nerve optic sheath. Sug-Radiol-Anat. 1966;18(4):323-328 23-Jinkins, J.R., Athale, S., Xiong, L , Yuh, W, T., Rothman, M.I., Nguyen, P. T. MR of the papilla protrusion in patients with high intracraneal pressure. AJNR-Am-J. Neuroradiol. 1966; 17(4):665-668 24-Quincke,H. Ueber meningitis serosa und verwandte. Zustande. Deutsch Z. Nervenheilk. 1987; 9:149 25- Bavetta, S; Sutcliffe, J.C., Sparrow, O.C., Hamlyn, P.J. A prospective comparison of fiber-optic and fluid-filled single lumen bolt subdural pressure transducers in ventilated neurosurgical patients. Br-J-Neurosurg. 1996 Jun; 10(3): 279-8 26- Buki-B; Avan-P; Lemaire-JJ; Dordain-M; Chazal-J; Ribari-O.: Otoacoustic emissions: a new tool for monitoring intracraneal pressure changes through stapes displacements. Hear-Res. 1996 May; 94(1-2): 125-39 27-Wilkinson, H A. :Intracraneal pressure. In. Youmans, J.R.: Neurological Surgery. 4th Edition, 1996; Vol.2 :66-695 28-Miller,J.D. Volume and pressure in the craniospinal axis. Clin.Neurosurg. 1975; 22:76-105 29-Hammer, J., Alberti, E., Hoyer, S. Influence of systemic and cerebral vascular factors on the cerebrospinal fluid pulse waves. J. Neurosurg. 1977; 46:36-45 30- Battro, A., Segura, R.G., Elicabe, C.A. Influence od respiration on blood pressure in man with a note on vasomotor waves. Arch. Intern. Med. 1944; 73:29-40 31-Miller, J. D., Butterworth, J.F.,Gudeman, S. K. Further experience in the manegment of severe head injury. J. Neurosurg. 1981; 54:289-299 32-Nornes, H., Magnaes, B. intracraneal pressures in patients with ruptured saccular aneurysm. J. Neurosurg. 1972; 36:537-547 33-Miller, J.D.: Intracranial pressure monitoring. Br.J. Hosp. Med. 1978; 19:497-503 34-Hayashi, M., Kobayashi, H., Handa,.Y. Brain blood volume and blood flow in patients with plateau waves. J. Neurosurg. 1985; 62:556-561 35-Risberg, J., Lundberg, N., Invarg, D. H. Regional cerebral blood volume during acute transient rises of the intracraneal pressure( plateau waves).J. Neurosurg. 1969; 31:310 36-Rosner, M.J.,Becker, D.P. Origin and evolution of plateau waves: Experimental observations and a theoretical model. J. Neurosurg. 1984; 60:312-324 37-Martin, G. Lundberg’s B waves as a feature of normal intracraneal pressure. Surg. Neurol. 1978; 9:347-348 38-Newell, D. W., Aaslid, R., Stooss, R. The relationship of blood flow velocity fluctuations to intracraneal pressure B waves. J. Neurosurg. 1992; 76:415-421 39- Dearden, N.M.: Intracranial pressure monitoring. Care Critically III 1985; 1: 8-13 40- Bradbury, M.W.B., Cole, D.F. The role of the lymphatic system in drainage of cerebrospinal fluid and aqueous humor. J Phisiol. 1980; 299: 353-365 41- Maset, A., Marmarou, A. Ward, J.D. Pressure Volume Index in Head Injury. J. Neurosurg. 1987; 67:832-840 42- Wilkinson, H. A., Arredondo, D., Weems, S. Intracraneal presssure reserve testing: A study in experimental animals. Arch.Neurol. 1978; 35: 567-576 43- Yundt, K.D., Diringer, M.N. The use of hyperventilation and its impact on cerebral ischemia in the treatment of traumatic brain injury. Crit-Care-Clin. 1997 Jan; 13(1): 163-84 44- DeSalles, A.A.F., Kontos, H.A., Becker, D.P. Prognostic significance of ventricular CSF lactic acidosis in severe head injury. J. Neurosurg. 1986; 65:615-624 45-Manitol-Muizelaar, J.P., Litz, H.A., Becker, D.P. Efect of mannitol on ICP and CBF and correlation with pressure autorregulation in severely head-injury patients. J. Neurosurg. 1984; 61: 700-706 46- Clarke-J.P. The effects of inverse ratio ventilation on intracraneal pressure: a preliminary report. Intensive-Care-Med. 1997 Jan; 23(1): 106-9 47- Geraci,E., Geraci, T. A look at recent hyperventilation studies: outcomes and recommendations for early use in the head-injured patient. J-Neurosci-Nurs. 1996 Aug; 28(4): 222-4, 229-33 48- Shackford-S.R. Effect of small-volume resuscitation on intracraneal pressure and related cerebral variables. J-Trauma. 1997 May; 42(5 Suppl): S48-53 49- Anderson,J.T., Wisner,D.H., Sullivan,P.E., Matteucci,M., Freshman,S., Hildreth,J., Wagner,F.C. Jr. Initial small-volume hypertonic resuscitation of shock and brain injury: short- and long-term effects. J-Trauma. 1997 Apr; 42(4): 592-600; discussion 600-1 50- Kirkpatrick,P.J., Smielewski,P., Piechnik,S., Pickard,J.D., Czosnyka,M.: Early effects of mannitol in patients with head injuries assessed using bedside multimodality monitoring. : Neurosurgery. 1996 Oct; 39(4): 714-20; discussion 720-1 51- Brain Trauma Foundation. The use of mannitol in severe head injury. J-Neurotrauma. 1996 Nov; 13(11): 705-9 52- Hartl,R., Ghajar,J., Hochleuthner,H., Mauritz,W.: Treatment of refractory intracranial hypertension in severe traumatic brain injury with repetitive hypertonic/hyperoncotic infusions. Zentralbl-Chir. 1997; 122(3): 181-5 53- Brain Trauma Foundation. The role of glucocorticoids in the treatment of severe head injury. J-Neurotrauma. 1996 Nov; 13(11): 715-8 54- Schoeman,J.F., Van-Zyl,L.E., Laubscher.J.A., Donald,P.R. Effect of corticosteroids on intracranial pressure, computed tomographic findings, and clinical outcome in young children with tuberculous meningitis. Pediatrics. 1997 Feb; 99(2): 226-31 55- Net Castel, A: Barbituricos a dosis altas en el traumatismo craneoencefalico grave. Neurologia. 1988; Vol 3: 209-210 56-Schwab,S., Spranger,M., Schwarz,S., Hacke,W. Barbiturate coma in severe hemispheric stroke: useful or obsolete?. : Neurology. 1997 Jun; 48(6): 1608-13 57-Russo, H., Bressolle,F., Duboin,MP. Pharmacokinetics of high-dose thiopental in pediatric patients with increased intracranial pressure. Ther-Drug-Monit. 1997 Feb; 19(1): 63-70 58- Brain Trauma Foundation. The use of barbiturates in the control of intracranial hypertension. J-Neurotrauma. 1996 Nov; 13(11): 711-4 59- Schwartz,A.E., Stone,J.G., Finck,A.D., Sandhu,A.A., Mongero,L.B., Adams,D.C., Jonassen,A.E., Young,W.L. Michler,R.E. Isolated cerebral hypothermia by single carotid artery perfusion of extracorporeally cooled blood in baboons. Neurosurgery. 1996 Sep; 39(3): 577-81; discussion 581-2 60- Bundgaard,H., Jensen,K.A., Cold,G.E., Bergholt,B., Frederiksen,R.O., Pless,S. Effect of indomethacin on the intracranial pressure. Ugeskr-Laeger. 1997 Jun 30; 159(27): 4261-5 61- Imberti,R., Bellinzona,G., Ilardi,M., Bruzzone,P., Pricca.P. The use of indomethacin to treat acute rises of intracranial pressure and improve global cerebral perfusion in a child with head trauma. Acta-Anaesthesiol-Scand. 1997 Apr; 41(4): 536-40 62- Bundgaard,H., Jensen,,K., Cold,G.E., Bergholt,B., Frederiksen,R., Pless.S. Effects of perioperative indomethacin on intracranial pressure, cerebral blood flow, and cerebral metabolism in patients subjected to craniotomy for cerebral tumors. J-Neurosurg-Anesthesiol. 1996 Oct; 8(4): 273-9 63-Jensen,K.A., Christensen,S.K., Nielsen,E.M., Bunemann,L.K., Therkelsen,K., Knudsen,F. Cerebral blood flow and indomethacin. The effect of different doses administered as continuous intravenous infusions or as suppositories in healthy adults. Ugeskr-Laeger. 1997 Jun 30; 159(27): 4257-60 64- Dahl,B., Bergholt,B., Cold,G.E., Astrup,J., Mosdal,B., Jensen,K., Kjaersgaard,J.O. CO(2) and indomethacin vasoreactivity in patients with head injury. Acta-Neurochir-Wien. 1996; 138(3): 265-73 65- Rockswold, G.L., Ford S.E., Anderson, D.C. Results of a prospective randomized trial for treatment of severely brain injured patients with hyperbaric oxygen. J. Neurosurg. 1992; 76: 929-934 66- Bagley,R.S., Harrington,M.L., Pluhar,G.E., Keegan,R.D., Greene,S.A., Moore,M.P., Gavin,P.R. Effect of craniectomy/durotomy alone and in combination with hyperventilation, diuretics, and corticosteroids on intracranial pressure in clinically normal dogs. Am-J-Vet-Res. 1996 Jan; 57(1): 116-9 |